Der vulnerable Patient mit Diabetes mellitus
Arbeitsgruppen Univ.-Prof. Dr. med. Nikolaus Marx
Univ.-Prof. Dr. med. Nikolaus Marx
Direktor der Klinik für Kardiologie, Angiologie und Internistische Intensivmedizin (Medizinische Klinik I)
Publikationen: For a complete reference list please see PubMed* Link
Uniklinik RWTH Aachen
Pauwelsstraße 30
52074 Aachen
Tel.: 0241 80-89300
Fax: 0241 80-82545
nmarxukaachende
Seit Jahren befassen sich verschiedene Arbeitsgruppen innerhalb der medizinischen Klinik I mit dem Thema „Der vulnerable Patient mit Diabetes mellitus“.
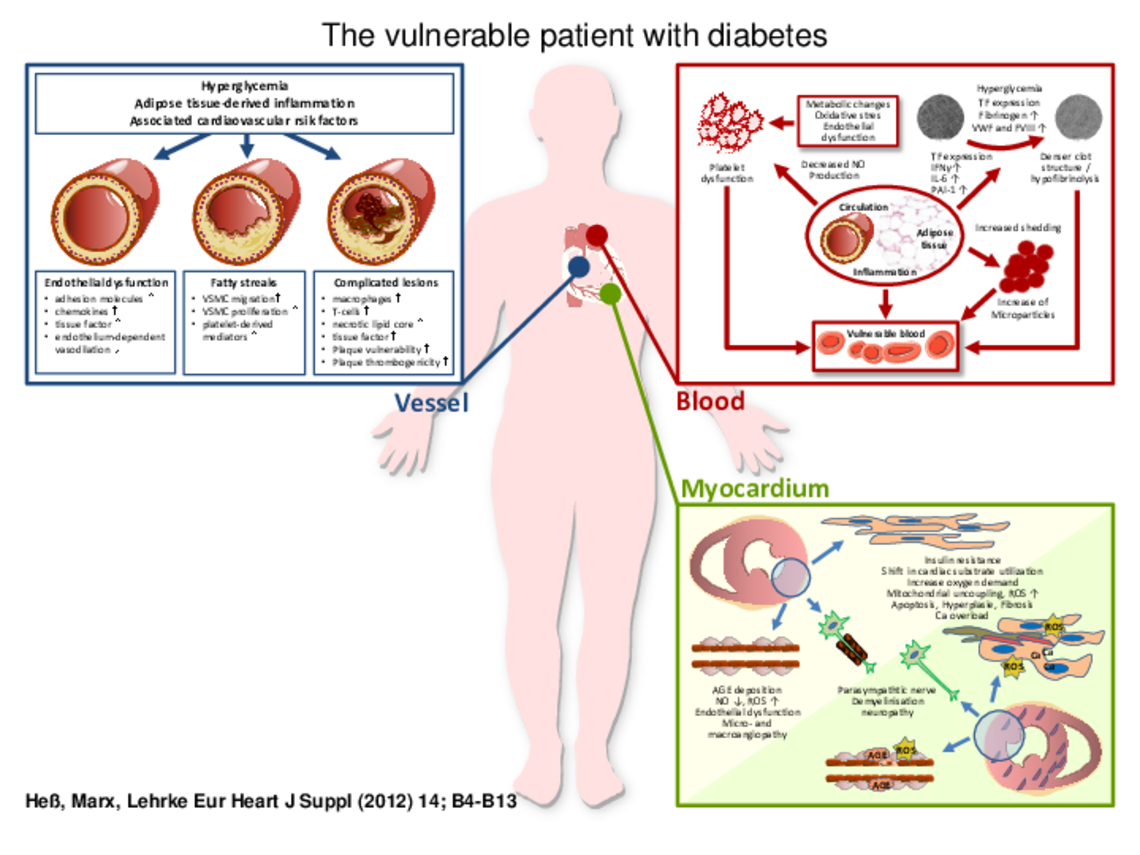
Patienten mit Diabetes mellitus haben ein erhöhtes Risiko für die Entwicklung einer Atherosklerose mit ihren Folgeerkrankungen akutem Myokardinfarkt, Schlaganfall oder Herzinsuffizienz. Für Jahrzehnte galt die Entwicklung instabiler atherosklerotischer Plaques mit Plaqueruptur und konsekutiver Thrombusentwicklung als einzige entscheidende Ursache der Entstehung akuter vaskulärer Ereignisse. Neuere Daten legen nahe, dass nicht alleine Veränderungen in der Gefäßwand hier ursächlich bedeutsam sind, sondern auch Veränderungen des Blutes und des Myokards selber von entscheidender Bedeutung sind. Somit charakterisieren diese drei Komponenten – vulnerables Gefäß, vulnerables Blut und vulnerables Myokard – den sogenannten kardiovaskulär vulnerablen Patienten. Patienten mit Diabetes mellitus sind kardiovaskulär vulnerable Patienten, da sie Veränderungen der Gefäßwand, des Blutes und des Myokards aufweisen. Verschiedene experimentell und translational arbeitende Gruppen analysieren diese Aspekte des vulnerablen Patienten mit dem Ziel, die Pathophysiologie und das Zusammenspiel der unterschiedlichen Komponenten besser zu verstehen und hieraus neue Therapiekonzepte abzuleiten.
- Metabolische Ursachen kardiovaskulärer Erkrankungen -
Prof. Dr. med. Michael Lehrke (stellvertretender Klinikdirektor)
Tel.: 0241 80-35136
Fax: 0241 80-82153
mlehrkeukaachende
Publikationen: For a complete reference list please see PubMed* Link
Die Arbeitsgruppe beschäftigt sich mit den metabolischen Ursachen kardiovaskulärer Erkrankungen. Hierbei liegt ein besonderes Augenmerk auf der Störung des Glukosestoffwechsels als Ursache von Atherosklerose und Kardiomyopathie. Als einen Schwerpunkt beschäftigen wir uns mit der Wirkung der Inkretinhormone GLP-1 und GIP auf das kardiovaskuläre System. Beide Inkretinhormone werden nahrungsabhängig aus endokrinen Zellen der Darmwand freigesetzt und verbessern Glukose-abhängig die Insulinausschüttung aus den pankreatischen Betazellen. Darüber hinausgehend besitzt GLP-1 kardiovaskuläre Wirkungen und reduziert sowohl die Gefäßwand-Inflammation im Rahmen einer Atherosklerose und wirkt darüber hinausgehend kardioprotektiv bei akutem Myokardinfarkt als auch diabetischer Kardiomyopahtie.
Ein weiterer Fokus liegt auf der Bedeutung des viszeralen Fettgewebes für die Entstehung von Atherosklerose und Kardiomyopahtie.
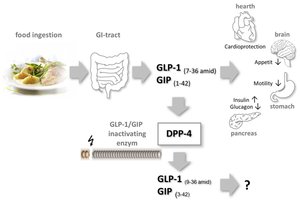
Schema der Sekretion, Metabolisierung und Wirkung der Inkretinhormone GLP-1 und GIP. Abbildung oben als PDF
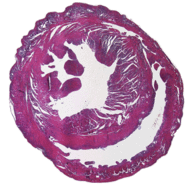
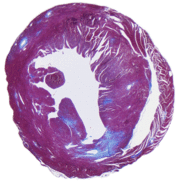
Kollagenfärbung eines normalen Herzens links sowie eines hypertrophierten Herzens rechts (Kollagen in blau).
- Gentherapeutische Ansätze zur Therapie kardiovaskulärer Erkrankungen -
Priv.-Doz. Dr. med. Corinna Lebherz (Oberärztin)
Tel.: 0241 80-35774
clebherzukaachende
Publikationen: For a complete reference list please see PubMed* Link
Kardiovaskuläre Erkrankungen stellen die häufigsten Krankheitsbilder in industrialisierten Staaten dar. Neue pharmakologische und/oder interventionelle Therapieansätze haben die Prognose der Patienten durch eine verbesserte Primär- und Sekundärprävention kardiovaskulärer Ereignisse sowie effektivere und schnellere Reperfusion verschlossener Koronararterien entscheidend verbessert. Trotzdem sind kardiovaskuläre Erkrankungen in westlichen Ländern weiterhin die Haupttodesursache, sodass gentherapeutische Therapieansätze auf diesem Gebiet zunehmend an Bedeutung gewinnen. Durch Fortschritte in der Grundlagenforschung sind mittlerweile viele Zielgene bekannt, die entweder direkt oder indirekt die Entstehung kardiovaskulärer Erkrankungen fördern oder inhibieren können. Dadurch ist eine Gentherapie nicht nur für angeborene Erkrankungen mit einem singulären Gendefekt – wie zum Beispiel der familiären Hypercholesterinämie –, sondern auch für multifaktoriell bedingte Erkrankungen denkbar. Ansatzpunkte zur Reduktion der Entstehung und Progression einer Atherosklerose bieten zum einen die klassischen Risikofaktoren wie der Diabetes mellitus oder die Hypercholesterinämie. Darüberhinaus sollen auch Einflüsse z.B. einer Niereninsuffizienz oder einer chronischen Inflammation berücksichtigt werden.
Bevorzugt werden von unserer Arbeitsgruppe virale Vektoren basierend auf Adeno-assoziierten Viren verwendet. Diese zeichnen sich durch ihre nur gering ausgeprägte Aktivierung des Immunsystems sowie eine stabile Genexpression aus. Durch Verwendung Gewebe-spezifischer oder regulierbarer Promotoren kann die Expression zudem gezielt eingesetzt werden. Ziel ist es, mittels viralem Gentransfer im Krankheitsprozess relevante Zielgene zu identifizieren und hierüber alternative Therapiestrategien aufzuzeigen und einzusetzen.
Adeno-assoziierter viraler Gentransfer ermöglicht Regulation des Gens durch exogene Liganden. Stabile Genexpression über mehr als 2 Jahre.
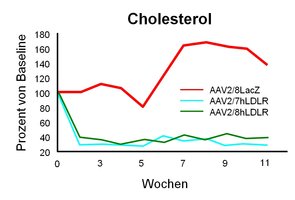
Gentransfer des LDL Rezeptors reduziert Cholesterin in einem Mausmodell für familiäre Hypercholesterinämie
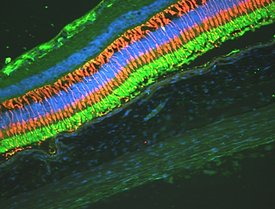
Erfolgreicher Gentransfer mit VEGF (grün) in der Retina
- Koronare Plaquevulnerabilität bei Hochrisikopatienten mit Typ 2 Diabetes: Prädiktoren und neue Therapieansätze -
Prof. Dr. Dr. med. Mathias Burgmaier (Oberarzt)
Tel.: 0241 80-36304
Fax: 0241 80-3336304
mburgmaierukaachende
Publikationen: For a complete reference list please see PubMed* Link
Nicole Krott (Medizinisch Technische Assistentin)
Tel.: 0241 80 35099
nkrottukaachende
Simone Battermann (Assistenzärztin)
Tel.: 0241 80-89303
simone.battermannrwth-aachende
Patienten mit Diabetes mellitus haben ein erhöhtes Risiko für eine koronare Herzerkrankung und ihre mögliche Folgeerscheinung, den akuten Myokardinfarkt. Dieses erhöhte kardiovaskuläre Risiko von Patienten mit Typ 2 Diabetes basiert vor allem auf der hohen Wahrscheinlichkeit ihrer atherosklerotischen Läsionen zu rupturieren und einen thrombotischen Gefäßverschluss zu verursachen. Entsprechend konnte in neueren Arbeiten gezeigt werden, dass die koronaren Läsionen von Patienten mit Typ 2 Diabetes im Vergleich zu Individuen ohne Diabetes vermehrt vulnerable Plaques aufweisen.
Ziel der AG Burgmaier ist es, 1. neue, nichtinvasive Prädiktoren für das Vorhandensein von vulnerablen Plaques bei Hochrisikopatienten mit Typ 2 Diabetes zu entwickeln und 2. neue Therapieansätze für die Behandlung von vulnerablen Plaques zu entwickeln.
1. Prädiktoren für vulnerable Plaques (AG Burgmaier und AG Reith): Zurzeit existieren keine klinisch genutzten Prädiktoren für die Erkennung von vulnerablen Plaques. Dabei ist die Risikoeinschätzung besonders bei Patienten mit Typ 2 Diabetes und ihrem hohen kardiovaskulären Risiko besonders wichtig. Hierzu wird in großen klinischen Studien die koronare Plaquemorphologie in Patienten mit und ohne Diabetes mittels optischer Kohärenztomographie (OCT) untersucht und der Zusammenhang mit verschiedenen klinischen, bildmorphologischen und laboranalytischen Parametern geprüft. OCT stellt derzeit in klinischen Studien den Goldstandart zur Erkennung von vulnerablen Plaquecharakteristika dar und erlaubt die Darstellung der koronaren Plaquemorphologie im Patienten mit der zurzeit höchsten Auflösung. Dieser Forschungsschwerpunkt profitiert von der optimalen interdisziplinären Zusammenarbeit der AG Burgmaier (Schwerpunkt Molekulare Kardiologie und translationale Forschung) und der AG Reith (Schwerpunkt Interventionelle Kardiologie und neue intrakoronare Bildgebungen), die in enger Zusammenarbeit diese Studien durchführen.
2. Neue Therapieansätze für vulnerable Plaques: Abgesehen von Statinen existieren keine klinisch genutzten Strategien zur Behandlung von vulnerablen Plaques. Dabei sind Behandlungskonzepte für die Therapie von vulnerablen Plaques bei Hochrisikopatienten mit Typ 2 Diabetes besonders relevant. Unter Ausschöpfung der gesamten Bandbreite der Grundlagenforschung wird hier in den verschiedensten in vitro Modellen der Effekt von Medikamenten auf Mechanismen untersucht, die einer Plaquestabilisierung zugrunde liegen. In unterschiedlichen Mausmodellen wird dann untersucht, ob diese Medikamente auch in vivo einen Effekt auf die Plaquevulnerabilität haben.
Priv.-Doz. Dr. med. Katharina Schütt (Oberärztin)
Tel.: 0241 80-37128
kschuettukaachende
Publikationen:
Katharina Schütt: For a complete reference list please see PubMed* Link and Katharina Heß: For a complete reference list please see PubMed* Link
Patienten mit Diabetes mellitus oder chronischer Nierenerkrankung haben ein deutlich erhöhtes kardiovaskuläres Risiko. Ein Grund hierfür sind Veränderungen in der Struktur und Lyse von Fibringerinnseln. So weiß man, dass die bei diesen Patienten auftretenden dünneren Fasern, kleineren Poren und die längere Lysezeit mit einem erhöhten kardiovaskulären Risiko assoziiert ist. Entzündliche Mechanismen scheinen hier eine entscheidende Rolle zu spielen. Die Grundlagen-orientierte Arbeitsgruppe untersucht die Rolle inflammatorischer Mediatoren auf die Fibringerinnsel sowie potentielle Interaktionsmöglichkeiten und die Wirkung neuer Antikoagulantien
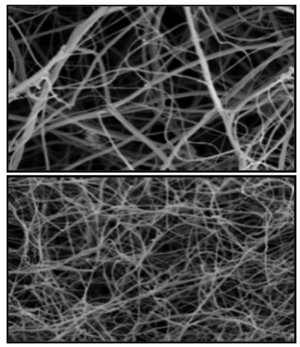
Elektronenmikroskopie zweier Fibringerinnsel. Oben gesunde Kontrolle unten Diabetiker.