Wissenschaft
Die wissenschaftliche Forschung der Klinik für Pneumologie und internistische Intensivmedizin deckt weite Teile des Spektrums der Pathogenese und Therapie pneumologischer Erkrankungen ab. Auf den folgenden Seiten informieren wir Sie über die Forschungsgebiete und die in ihnen tätigen Arbeitsgruppen sowie über Kooperationsprojekte mit Forschungsrotation und die Beteiligung unserer Klinik an klinischen Studien.
Intensiv- und Beatmungsmedizin
Die Arbeitsgruppe um Univ.-Prof. Dr. med. Michael Dreher beschäftigt sich mit der Forschung im Bereich der Intensiv- und Beatmungsmedizin sowie der Entwöhnung vom Respirator (Weaning). Genauere Informationen über den wissenschaftlichen Schwerpunkt finden Sie unter folgendem Link: PUPMED.
Beispielhaft seien hier zwei Projekte genannt: Das DIGIVENT und das HOME-VENT Projekt. Bei dem DIGIVENT Projekt handelt es sich um ein vom Bundesministerium für Bildung und Forschung (BMBF) gefördertes Projekt, bei dem unsere Klinik Projektpartner ist. Das Projekt dient der Entwicklung und Erprobung eines Digitalen Therapieunterstutzungssystems in der außerklinischen Beatmung bei COPD-Patienten. Details sind der entsprechenden offiziellen Pressemitteilung zu entnehmen. Die HOME-VENT Studie dient dem Zweck der Erforschung der Compliance der Nutzung einer Heimbeatmung bei Patienten mit fortgeschrittener COPD und der Erforschung zum Einsatz moderner Tele-Monitoring Systeme, um die Compliance hin zur effektiveren Nutzung dieser Heimbeatmungstherapie bei diesen Patienten zu steigern. Details zu dieser Studie (Principal Investigator: Michael Dreher) sind der Studien ID sowie einem Webinar der European Respiratory Society (ERS) zu entnehmen.
Für Rückfragen steht Ihnen Univ.-Prof. Dr. med. Michael Dreher unter folgender E-Mail-Adresse: mdreherukaachende zur Verfügung.
Sedierung im Rahmen von Bronchoskopien
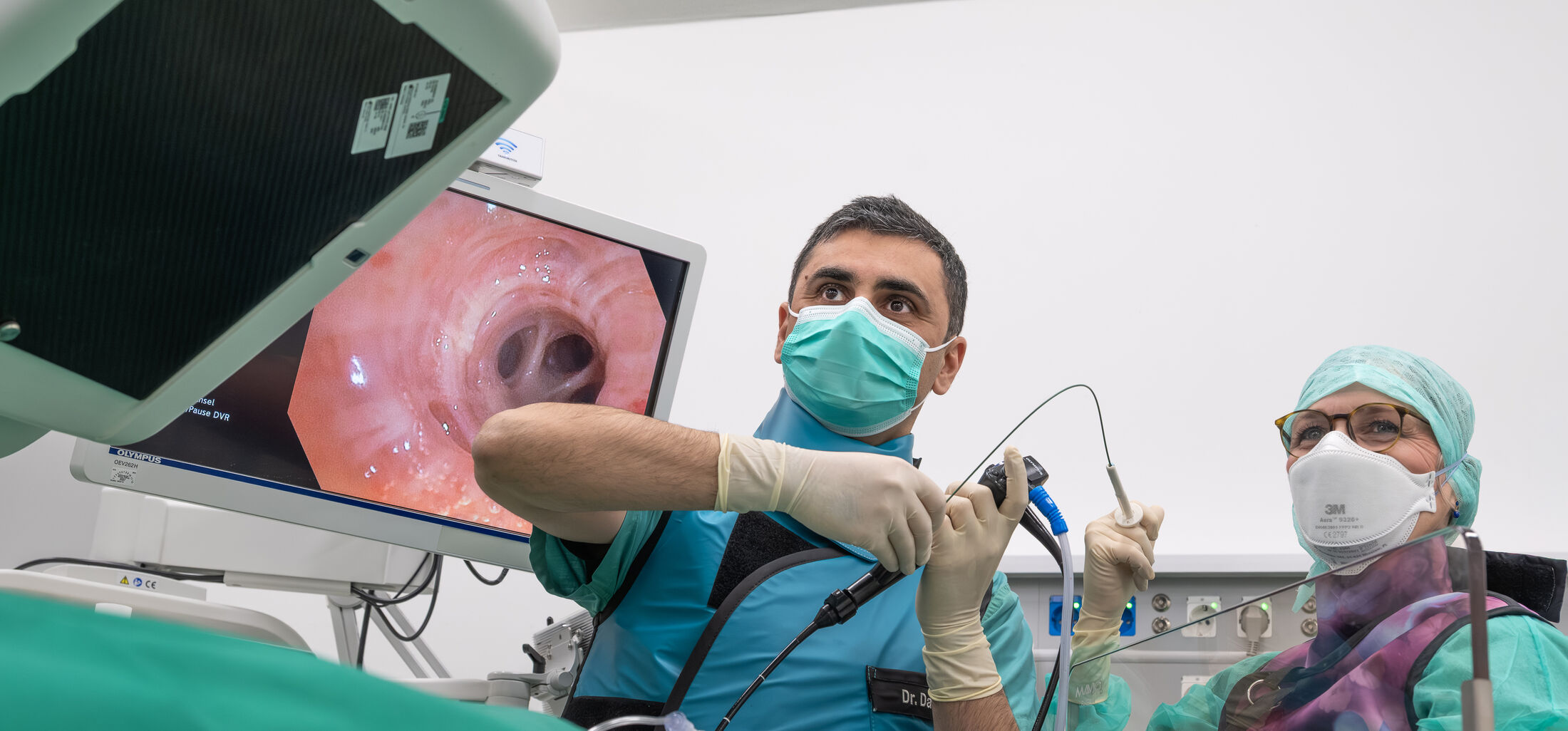
Laufende klinische Studien unter der Verantwortung von Priv.-Doz. Dr. med. Tobias Müller beschäftigen sich mit der optimalen Sedierung von Patienten im Rahmen von Lungenspiegelungen (Bronchoskopien). Hierbei wird insbesondere untersucht, ob die Verabreichung von Lokalanästhetika über spezielle Zerstäubersysteme zu einer schonenderen Untersuchung für den Patienten führt.
Für Rückfragen:
Priv.-Doz. Dr. med. Tobias Müller
tobmueller@ukaachen
Respiratorisches Tissue Engineering
Die Forschungsaktivitäten der Arbeitsgruppe „Respiratorisches Tissue Engineering“ des Lehr- und Forschungsgebietes „Biohybrid and Medical Textiles“ konzentrieren sich auf die Entwicklung biohybrider Systeme und Verfahren zur Zelltherapie, um die Funktion der Atemwege und Lunge zu wiederherzustellen oder zu ersetzen.
So entwickeln wir im Projekt PulmoStent einen biohybriden Atemwegsstent, um die Lebensqualität von Patienten mit Lungenkrebs zu verbessern. Im EndOxy-Projekt entwickeln wir eine biohybride Lunge, die Patienten mit lebensbedrohlichem Lungenversagen eine langfristige Lungenunterstützung ermöglicht. Für diese Indikation entwickeln wir außerdem neue Verfahren zur Zelltherapie, um die Regenerationsvorgänge der Lunge zu unterstützen.
Weitere Informationen zu unseren Forschungsprojekten im Bereich Tissue Engineering finden Sie auf der Website des Instituts für Angewandte Medizintechnik.
Leitung: Priv.-Doz. Dr. Christian Cornelissen & Dr. Lena Thiebes
Kardio-Pulmonale Interaktion
Mit Eröffnung der interdisziplinären pneumologisch-kardiologischen Normalstation IM 12 wurde gleichzeitig ein neuer wissenschaftlicher Schwerpunkt im Bereich der kardio-pulmonalen Interaktion gegründet. Dies erscheint unter dem Gesichtspunkt einer hohen kardialen Komorbidität bei Lungenerkrankung sowie einer hohen pulmonalen Komorbidität bei kardialen Erkrankungen sinnvoll.
Zusätzlich ist ein wesentliches Kardinalsymptom beider Fachbereiche die Luftnot und es ist oft schwierig, dieses breite Symptom der ein oder anderen Erkrankung genau zuzuordnen. Der wissenschaftliche Schwerpunkt der kardio-pulmonalen Interkation versucht, den Zusammenhang zwischen pulmonaler und kardialer Funktion bei unterschiedlicher Erkrankungen genauer zu untersuchen.
Für Rückfragen:
PD Dr. med. Ayham Daher
adaherukaachende
Atmungs- und Beatmungsphysiologie, Translationale Pneumologie
Wir freuen uns über Ihr Interesse an unserer Arbeitsgruppe und stehen bei Rückfragen unter unten genannten Kontaktmöglichkeiten gerne zur Verfügung.
Den Kern unserer Arbeitsgruppe bildet ein Labor für die Physiologie der Atmung und des autonomen Nervensystems (engl. Translational Respiratory Autonomic Nervous System Physiology Laboratory, Aachen; TRANSPARENT-Lab) mit Möglichkeit zur Erhebung und Analyse einer Reihe von experimentellen atmungsphysiologischen und kardiovaskulären Variablen. Die invasive Erfassung und Messung des Sympathikotonus (sog. Muscle sympathetic nerve activity, MSNA) nach externer und intraneuraler Mikrostimulation und auch im Blut nachweisbare Biomarker dessen (w.z.B. Katecholamine) sowie die Messung der zentralen und peripheren Chemosensitivität sind dabei in unserem Labor genauso etabliert wie die invasive Erfassung der Atemmuskelkraft mittels Ballonkathetern und in Reaktion auf supramaximale kortikale und zervikale magnetische phrenicus Nerv Stimulation (sog. Twitch transdiaphragmatic pressure Erfassung und Analyse).
Methodik und Inhalte unserer translationalen Forschungs-Projekte auf dem Gebiet der Atmungs- und Beatmungs-physiologie bei Patienten mit pulmonaler Hypertonie (sowie systolischer Herzinsuffizienz) einerseits und Patienten mit COPD und neuromuskulären Erkrankungen andererseits knüpfen dabei direkt an Vorarbeiten der Arbeitsgruppenleitung am Universitätsklinikum Aachen um PD Dr. med. Jens Spiesshoefer aus einem Clinician Scientist Programm am Universitätsklinikum Münster in einem entsprechenden Labor für Atmungsphysiologe (Arbeitsgruppe am Universitätsklinikum Münster: AG PD Dr. med. Matthias Boentert, Klinik für Neurologie, vormals Schlafmedizin) an.
Elementarer Bestandteil der Arbeitsgruppe ist der Austausch in einem gut etablierten internationalen Netzwerk u.a. um das Institute of Life Sciences der Scuola Superiore Sant Anna Pisa, Italien (Prof. Alberto Giannoni, Prof. Claudio Passino und Prof. Michele Emdin) und das Human Autonomic Neurophysiology Laboratory des Baker Heart Institutes Melbourne (Monash University Melbourne), Australien (Prof Vaughan Macefield) Prof. Hans Joachim Kabitz (Klinikum Konstanz und Universität Freiburg;) und am National Heart and Lung Institute London (Imperial College London).
Unsere Arbeitsgruppe arbeitet methodisch und inhaltlich auf zwei Gebieten:
Das folgende Video eines Vortrages von PD Dr. Dr. med. Jens Spiesshoefer als invited keynote speaker am Toronto General Hospital fasst die aktuellen Aktivitäten der Gruppe und des Labors auch zusammen:
1. Atmungsphysiologie bei pulmonale Hypertonie und Herz-Insuffizienz Patienten
Im Rahmen einer Reihe von Projekten untersuchen wir die Pathophysiologie der Chemoreflexe sowie (schlafbezogener) Atmungsstörungen bzw. dem hypoxischen Atemversagen und Ihrer Therapie bei Patienten mit präkapillärer pulmonaler Hypertonie (PH) sowie bei Patienten mit systolischer Herzinsuffizienz (HFrEF).
Der Sympathikotonus ist seit Jahren pathophysiologisches Therapie-Ziel einer Reihe von nun Leitlinien empfohlener Pharmakotherapien (u.a. Beta-Blocker Therapie und Therapie mittels Funny Channel Inhibitors) von Patienten mit HFrEF und ist zunehmend auch zumindest Forschungsgegenstand bei Patienten mit PH. Die muskulär sympathische nerven Messung (MSNA-Messung) ist der Goldstandard der Sympathikotonus Erfassung im Menschen. Dabei wird vorsichtig eine kleine Nadel auf Unterschenkel-Höhe in einen Nerven eingeführt. Über Aufzeichnung der Entladungsrate dieses Nervens können so wertvolle Rückschlüsse auf den „Stress“ für den Körper gezogen werden. Diese invasive d.h. “eindringende” Untersuchung ist aber nur in wenigen Zentren weltweit (u.a. eben Pisa, Italien und Melbourne Australien) und nun als einem der wenigen Standorte in Deutschland der Aachener Unversitätsmedizin verfügbar. Dabei kommt neben der Erfassung der MSNA die Erfassung des Blutdruckes, der Herzfrequenz und Blutdruckvariabilität sowie der Barorezeptorreflexsensitivität zum Einsatz (Abbildung 1).
Bei Patienten mit HFrEF und auch PH soll In Kooperation mit dem Institute of Life Sciences der Scuola Superiore Sant Anna Pisa (Prof. Alberto Giannoni, Prof. Claudio Passino und Prof. Michele Emdin) ein Modell der Sympathikotonus Erhöhung erstellt werden hier mit Fokus auf die Atemregulatons also Chemoreflex Veränderungen und die Cheyne-Stokes Atmung (Abbildung 2). Die Cheyne Stokes Atmung mit zentralen Apnoen nachts und am Tage ist hochprävalent bei Patienten mit HFrEF, von prognostischer Bedeutung und eng mit einem erhöhten zentralen Atemantrieb verbunden (sog. CO2 Chemosensitivität; in unserem Labor ebenfalls messbar in Form von der Messung der hypoxischen -HVR- und hyperkapnischen -HCVR- Atemantwort). Umso erstaunlicher ist es, dass klinisch-therapeutische Bemühungen bei HFrEF Patienten sich in dieser Hinsicht bisher nur darauf fokussiert haben mittels Masken-basierter Therapien den Endpunkt dieser komplexen Pathophysiologie in Form von der Cheyne-Stokes Atmung anzugreifen. Daher soll zunächst eine entsprechende translationale Grundlage geschaffen werden der Verzahnung der Chemoreflexe (HCVR, HVR und Messung des Plant Gains als Determinanten der Cheyne-Stokes Atmung im Menschen) mit dem Sympathikotonus bei Patienten mit HFrEF (und PH) zu entschlüsseln. Dem sollen dann auch dezidierte Projekte folgen zur pharmakologischen Beeinflussung der Chemoreflexe (Hyperventilationsneigung und Neigung zur instabilen Atmung in Form von einer Cheyne Stokes Atmung) und damit dem Sympathikotonus und damit der Symptomatik von HFrEF und PH Patienten mittels zentral wirksamer Medikamente.
2. Atmungs- und Beatmungs-Physiologie bei COPD und neuromuskulären Patienten
Im Rahmen einer Reihe an Projekten in unserem Labor für die Physiologie der Atmung und des autonomen Nervensystems untersuchen wir die Pathophysiologie und innovative Diagnostik der Atemmuskelfunktion und damit (klinisch) sowohl von restriktiven (bei Patienten mit neuromuskulären Erkrankungen) als auch von obstruktiven Ventilationsstörungen (bei Patienten mit COPD).
Basierend auf der starken Mitarbeiterabhängigkeit aktuell klinisch genutzter Lungenfunktionsuntersuchungen haben wir in Anlehnung an entsprechende Vorarbeiten -u.a. von Professor Hans-Joachim Kabitz (Klinikum Konstanz und Universität Freiburg) mit dem unsere Arbeitsgruppe kooperiert- mitarbeiterunabhängige Lungenfunktions-Untersuchungsprotokolle entwickelt. Methodisch kommen dabei neben der sonographischen Untersuchung des Zwerchfelles vor allem die zervikale und kortikale Magnetstimulation der Nn. Phrenici mit invasiver Ableitung der transdiaphragmalen Druckunterschiede (pDIs) mittels Ballonkatheter sowie die Aufzeichnung der resultierenden Muskelaktionssummenpotenziale (cMAPs) zum Einsatz (Abbildung 3). Weiterhin kann mittels eines von uns optimierten Protokolls (sog. Twitch superimpositioning technique bzw. twitch occlusion technique sowie mittels EMG Ableitung motorisch evozierter Potentiale nach kortikaler Magnetstimulation der Nn. phrenici) auch die kortikale Kontrolle des Zwerchfelles als Hauptmuskel der Atemmuskelpumpe im Menschen gemessen werden. Diese invasive und nicht volitionale Goldstandard-Diagnostik der Atemmuskel (die in der Lungenfunktion und Hyperkapnie oft am Ende erst Ihren Ausdruck der eigentlichen Atemmuskelfunktion findet) und damit Lungenfunktion und Hyperkapnie im Menschen ist zurzeit in Deutschland nur am Universitätsklinikum Aachen verfügbar.
Dies soll gerade für den Bereich der neuromuskulären Erkrankungen u.a. in Kooperation mit der AG Boentert der Klinik für Neurologie mit Institut für Translationale Neurologie (Direktor: Univ.-Prof. Prof. h.c. Dr. med. Heinz Wiendl) bzw. dem Bereich Neurologie des UKM Marienhospitals Steinfurt erfolgen. Hier ergibt sich der translational hoch-relevante Aspekt der Entschlüsselung der komplexen Pathophysiologie der Atemmuskelkraft-Beteiligung und damit des hyperkapnischen Atemversagens bei einer Reihe von neuromuskulären Erkrankungen, hier vor allem den klinisch langsam voranschreitenden neuromuskulären Erkrankungen, bei denen dieser Aspekt zum Nachteil der Patienten pneumologisch-neurologisch noch immer (zu) wenig Beachtung findet.
Auf dem Gebiet der COPD bedeutet dies konkret, dass ein pathophysiologisches Modell der Atemmuskelkraft Einschränkung in Ihren Eigenschaften, Ihren Determinanten, Ihrem prognostischen Wert, Ihrem Verlauf sowie Ihrem Einfluss auf die Belastungsintoleranz erstellt werden soll. Unserem Verständnis nach korrelieren dabei die myopathischen Veränderungen der Atemmuskelfunktion bei COPD Patienten deutlich besser mit den Symptomen und der Prognose dieser als spirometrische Variablen w.z.B. die FEV1.
Ebenfalls von besonderem Interesse ist der mögliche Rückgang der Atemmuskelfunktion durch Inaktivität unter invasiver Beatmung bei COPD und anderen Beatmungspatienten. Hier wollen wir invasiv mittels Ballonkathetern und Magnetstimulationsprotokollen der Zwerchfellnerven kortikal und zervikal die Atemmuskelfunktion und Ihre neuronale Kontrolle über die Dauer der invasiven Beatmung hinweg erforschen, um Determinanten und Pathophysiologie einer möglichen Atrophie und Dysfunktion dieser künftig besser zu verstehen.
Translational ist hier bei ambulanten wie bei stationären (z.T. beatmeten) COPD Patienten von besonderem Interesse, dass gezielte therapeutische Strategien zur Verbesserung der Atemmuskelfunktion bei diesen Patienten in Form von gezieltem Atemmuskelkraft-Training aber auch in Form von Neuroimplantaten, die das Zwerchfell gezielt stimulieren bereits zur Verfügung steht, wir jedoch die richtige Zielgruppe sowie die zu erfassenden Endpunkte für diese Therapien bei COPD Patienten erst noch verstehen müssen.
Ein weiterer translationaler Ansatzpunkt aus einem besseren Verständnis der Atemmuskelfunktion bei COPD Patienten heraus entsteht unter Nutzung der o.g. „kardiovaskulären“ Methodik um die Erfassung von muskulär sympathischer Nervenaktivität. Hier sollen Erkenntnisse zur Atemmuskelfunktion bei COPD Patienten auch in den Kontext Ihrer kardiovaskulären Implikationen gesetzt werden. Konkret zeichnen sich sehr wahrscheinlich nicht nur PH und HFrEF (also „Herz“ Kranke) Patienten, sondern auch COPD Patienten durch einen erhöhten Sympathikotonus aus. Ein Verständnis der Determinanten (darunter mutmaßlich eben die Atemmuskelfunktion) und der Eigenschaften der Sympathikotnus Erhöhung bei COPD Patienten könnte dabei die Grundlage für gezielte therapeutische Interventionen im Sinne einer modernen Präzisionsmedizin liefern. Gerade der allumfassende Ansatz der Quantifizierung des Sympathikotonuses in unserem Labor ermöglicht eine Unterscheidung zwischen vasokonstriktiv wirkenden Anteilen des Sympathiktonus und zentral Herzfrequenz erhöhenden Anteilen des Sympathikotonus (Abbildung 1). Zu oben genannter Methodik und Inhalten der Arbeitsgruppe und des Labors konnte auch ein neues Wahlfach zur studentischen Lehre auf dem Gebiet der Atmungs-, Beatmungs-Physiologie an der medizinischen Fakultät der RWTH Aachen geschaffen werden (LA 002 Atmungs- und Beatmungsphysiologie).
Unser Team
AG- Leitung
Priv.-Doz. Dr. Dr. med. Jens Spiesshoefer, Facharzt für Innere Medizin und Pneumologie, Klinik für Innere Medizin V: Pneumologie und internistische Intensivmedizin, Uniklinik RWTH Aachen, Direktor: Univ.-Prof. Dr. med. Michael Dreher.
jspiesshoeferukaachende / jens.spiesshoefersantannapisait
Publikationen
Stellvertretender Arbeitsgruppenleiter:
Dr. med. Binaya Regmi (z.Zt. Forschungsaufenthalt Cambridge, UK)
bregmiukaachende
Publikationen

Lab Managerin
Sitraka Faniry Nantenaina Ratsimba, Study Nurse, B.Sc., M.Sc., PhD Student
sratsimbaukaachende
Wissenschaftliche Mitarbeiter:
Janina Friedrich
jafriedrichukaachende
Marvin Schmidt
marvschmidtukaachende
cand. med. Gonxhe Shala
gshaladiabeteszentrum-neussde
Felix Christian Wagner
fewagnerukaachende
Doktoranden
cand. med. Max Barth
maximilian.barthrwth-aachende
cand. med. Mustafa Elfeturi
mustafa.elfeturirwth-aachende
cand. med. Jonathan Enriquez-Geppert
jonathan.enriquez.geppertrwth-aachende
cand. med. Sophia Faller
sophia.fallerrwth-aachende
cand. med. Oscar Gorol
oscar.gorolrwth-aachende
cand. med. Paul Großekemper
paul.grossekemperrwth-aachende
cand. med. David Hidalgo
david.hidalgorwth-aachende
cand. med. Benedikt Jörn
bejoernukaachende
cand. med. Paulina Rach
paulina-doreen.rachmf.stud.vult
cand. med. Lorenz Schrader
lorenz.schraderrwth-aachende
cand. med. Mehdi Senol
mehdi.senolrwth-aachende
cand. med. Jan Thomer
jan.thomerrwth-aachende
cand. med. Samira Yousef
samira.yousefrwth-aachende
Studentische Hilfskraft
cand. med. Benedikt Jörn
bejoernukaachende
Kompetitiv eingeworbene Förderungen
2012-2016: Studienstiftung des deutschen Volkes (mit Auslands und Forschungsförderung) (Spiesshoefer)
2018-2020: Else Kröner-Fresenius-Stiftung (Spiesshoefer)
2018-2020: Kommission für Innovative Medizinische Forschung an der medizinischen Fakultät Münster (IMF) (Spiesshoefer)
2019-2020: Deutsche Herzstiftung (Spiesshoefer)
2022-2024: START Programm der medizinischen Fakultät der RWTH Aachen (Spiesshoefer)
Young Investigator Support, PhD Programme Translational Medicine, Curriculum System Physiology, Institute of Life Sciences, Scuola Superiore Sant Anna Pisa (Spiesshoefer)
[Industrie] (Spiesshoefer, Dreher)
2025-2027: Else Kröner Exzellenz-Stipendium (Spiesshoefer)
2026-2029: Deutsche Forschungsgemeinschaft (Spiesshoefer)
2025-2030: Gemeinsamer Bundesausschuss HIPACO 1 und 2 Trials (Dreher/Windisch/Spiesshoefer/Stanzel)
Kooperationen
National
Priv.-Doz. Dr. med. Matthias Boentert, Klinik für Neurologie mit Institut für Translationale Neurologie, Universitätsklinikum Münster (UKM) & Bereich Neurologie des UKM Marienhospitals Steinfurt
Prof. Dr. med. Hans Joachim Kabitz, Pneumologie und Schlafmedizin, Kantonsspital Aarau
Univ.-Prof. Dr. med. Wolfram Windisch, Klinik für Pneumologie, Klinikum Köln-Merheim | Lehrstuhl für Pneumologie, Universität Witten-Herdecke
Prof. Dr. med. Michael Arzt, Schlafmedizinisches Zentrum der Klinik und Poliklinik für Innere Medizin II Universitätsklinikum Regensburg, Regensburg
Prof. Dr. med. Winfried J. Randerath, Krankenhaus Bethanien, Klinik für Pneumologie und Allergologie und Institut für Pneumologie an der Universität zu Köln, Solingen
Dr. med. Simon Herkenrath, Krankenhaus Bethanien, Klinik für Pneumologie und Allergologie und Institut für Pneumologie an der Universität zu Köln, Solingen
Prof. Dr. med. Olaf Oldenburg, Clemens-Hospital Münster, Klink für Kardiologie, Münster
Prof. Dr. Dr.med. Gerhard-Paul Diller, Klinik für Erwachsene mit angeborenen und erworbenen Herzfehlern, Universitätsklinikum Münster, Münster
Priv.-Doz. Dr. med. Michael Mohr, Medizinische Klinik A, Universitätsklinikum Münster, Münster
Univ.-Prof. Dr. med. Ali Yilmaz, Klinik für Kardiologie, Universitätsklinikum Münster, Münster
PD Dr. med. Stephan Walterspacher, Studienzentrum Klinikum Konstanz , www.studienzentrum-bodensee.de und Praxis und akademische Lehrpraxis -www.lungenaerzte-singen.de
International
Professor Alberto Giannoni, Dept. of Cardiology and School of Advanced Studies at Fondazione Toscana G. Monasterio (CNR) Pisa and Institute of Life Sciences at Sant Anna School of Advanced Studies Pisa, Pisa | Professor (Assistant) Institute of Life Sciences at Sant Anna School of Advanced Studies Pisa, Pisa, Italy
Professor Vaughan Macefield, Head, Human Autonomic Neurophysiology (Baker Heart Institute, Melbourne, Australia) | BSc (Hons I) PhD DSc FAAS FRSN | Senior Principal Research Fellow, Professorial Fellow, Department of Physiology, University of Melbourne, Melbourne, Australia | Adjunct Professor Department of Neuroscience, Monash University, Melbourne, Australia | Professor of Physiology, Western Sydney University, Sydney, Australia |
Professor Michele Emdin, Director of Dept. of Cardiology and School of Advanced Studies at Fondazione Toscana G. Monasterio (CNR) Pisa | Professor (Full) Institute of Life Sciences at Sant Anna School of Advanced Studies Pisa, Pisa, Italy
Professor Claudio Passino, Dept. of Cardiology and School of Advanced Studies at Fondazione Toscana G. Monasterio (CNR) Pisa and Institute of Life Sciences at Sant Anna School of Advanced Studies Pisa, Pisa | Professor (Associate) Institute of Life Sciences at Sant Anna School of Advanced Studies Pisa, Pisa, Italy
Professor Michael Polkey, Head of Department of Respiratory Medicine, National Heart and Lung Center and Royal Brompton Hospital London, London UK and Professor (Full), Imperial College London
Professor Eline Mos-Oppersma, Twente
Professor Annemijn Jonkman, Rotterdam
Prof. Dr. med. Hans-Joachim-Kabitz, Klinik für Pneumologie und Schlafmedizin, Kantonsspital Aarau, Aarau, Schweiz
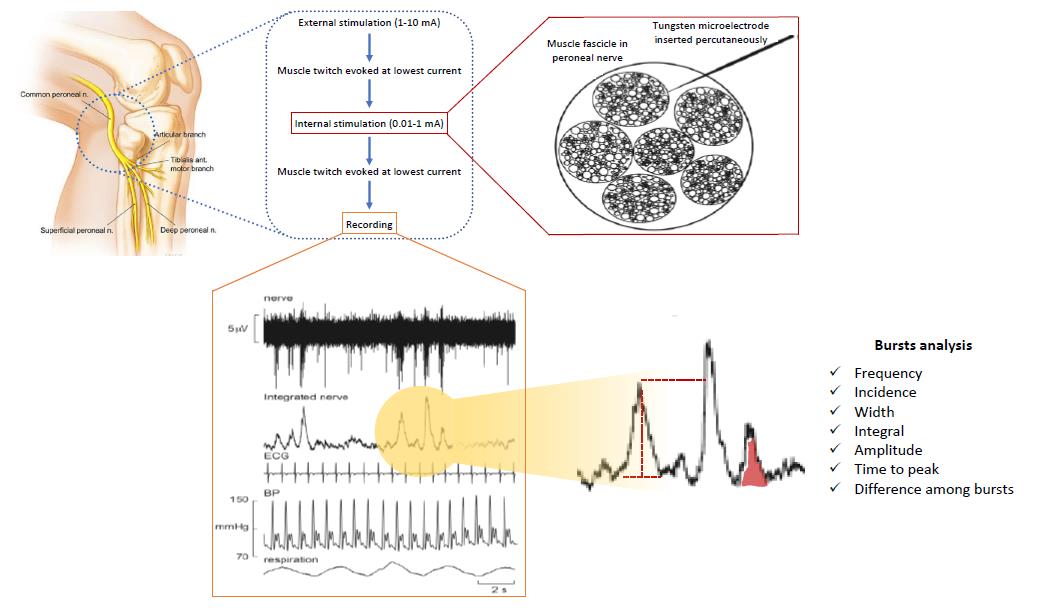
Abbildung 1
Abbildung 1. Invasive gold standard of the assessment of sympathetic nerve activity in humans. Multi-unit recording of muscle SNA following a standardized approach of external and intraneural microstimuafrom a healthy participant via a tungsten microelectrode inserted percutaneously into a muscle fascicle of the peroneal nerve, shown schematically on the left. Muscle SNA occurs as bursts with a clear cardiac rhythmicity. Heart rate and diastolic blood pressure variability can be derived from the setup used through ECG and continuous (finger) blood pressure all being recorded simultaneously.
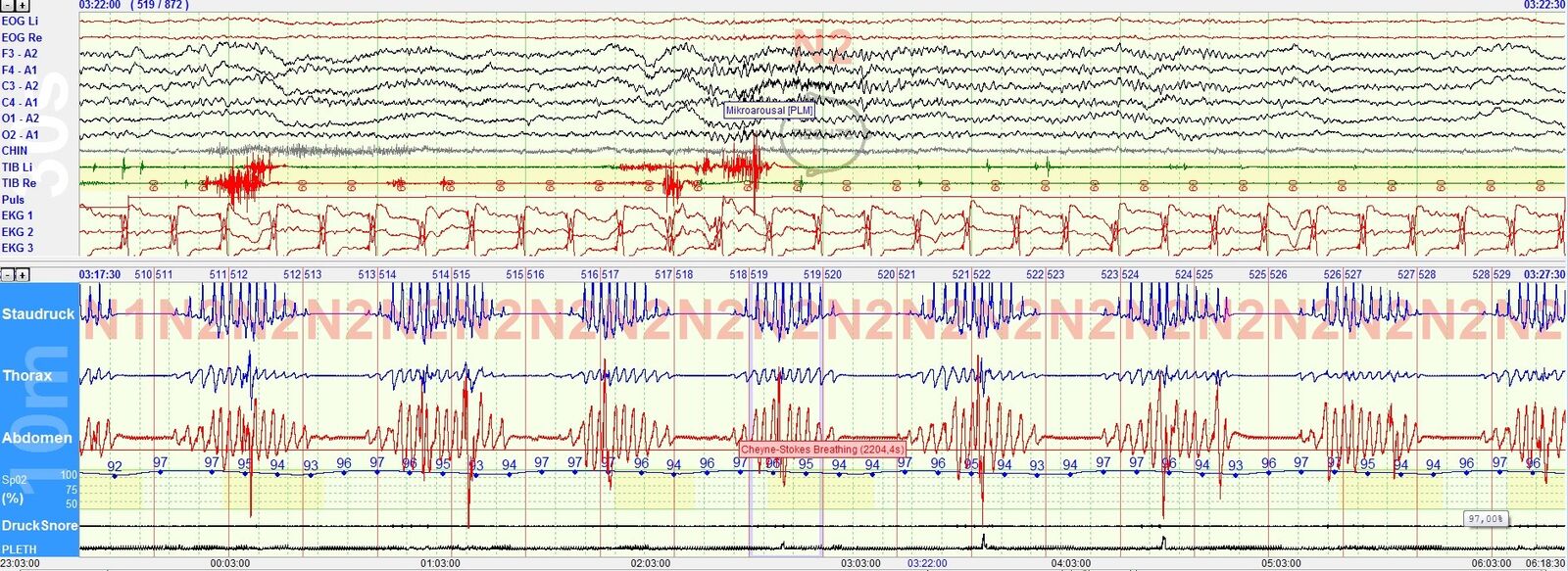
Abbildung 2
Abbildung 2: Polysomnographische Aufzeichnung einer Cheyne-Stokes Atmung bei einem Patienten mit systolischer Herzinsuffizienz im Tiefschlafstadium N2. Vergleiche von Markern des Sympathikotonus zwischen verschiedenen Maskenbasierten Therapien und (z.B. zentralen und obstruktiven) Atmungsstörungen nachts erlauben Rückschlüsse auf die kardiovaskulären Effekte und die optimale Therapie von Apnoen bei Patienten mit Herzinsuffizienz bzw. pulmonaler Hypertonie.
Siehe dazu auch: Gorbachevski, Spiesshoefer, Giannoni et al. Adaptive servo-ventilation therapy does not favourably alter sympatho-vagal balance in sleeping patients with systolic heart failure and central apnoeas: Preliminary data. International Journal of Cardiology 2020 & Spiesshoefer, Linz, Oldenburg et al. Sleep - the yet underappreciated player in cardiovascular diseases: A clinical review from the German Cardiac Society Working Group on Sleep Disordered Breathing. European Journal of Preventive Cardiology 2019.
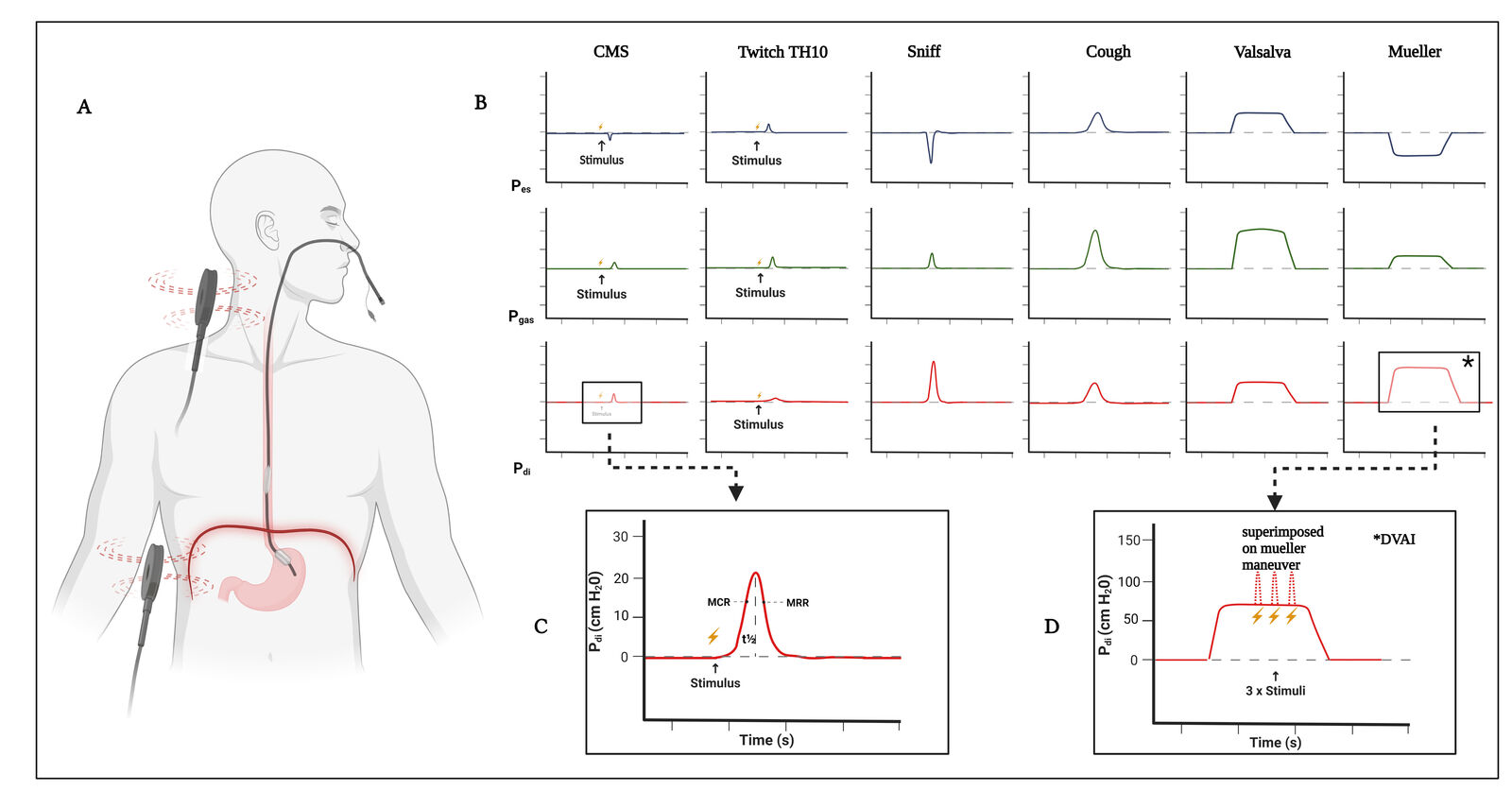
Abbildung 3
Abbildung 3: Magnetstimulation, invasive Atemmuskelkraft Messung per Goldstandard im Menschen und Twitch-Interpolation. Versuchsaufbau und repräsentative Messung.
Siehe dazu:
Regmi B, Friedrich J, Jörn B, Senol M, Giannoni A, Boentert M, Daher A, Dreher M, Spiesshoefer J.
Diaphragm Muscle Weakness Might Explain Exertional Dyspnea Fifteen Months After Hospitalization for COVID-19.
Am J Respir Crit Care Med. 2023 Jan 3. doi: 10.1164/rccm.202206-1243OC.
PMID: 36596223.
https://www.atsjournals.org/doi/abs/10.1164/rccm.202206-1243OC
Projekt: Arzneimitteltherapie-assoziierte Dyspnoe bei chronischen Atemwegserkrankung
Dyspnoe (Luftnot) als Leitsymptom sowie Vulnerabilitätsfaktor für das Vorliegen einer Nebenwirkung oder Arzneimittelwechselwirkung, insbesondere bei Patienten/-innen mit bereits bestehenden kardiopulmonalen Vorerkrankungen, ist bisher wissenschaftlich nicht hinreichend aufgearbeitet. In einer Kooperationsarbeit mit dem Institut für Klinische Pharmakologie unter Leitung von Fr. Prof. Dr. med. J. C. Stingl erforschen wir bisher unerkannte Wechselwirkungen und Risikomuster mit dem Ziel die Therapiesicherheit für Patienten/-innen zu steigern und individuelle Risiken im Sinne einer personalisierten Medizin zu reduzieren. Laufende Projekte befassen sich z.B. unter anderem mit Untersuchungen zu Arzneimittelnebenwirkungen/-wechselwirkungen als Vorstellungsgrund in deutschen Notaufnahmen.
Für weitere Informationen und Nachfragen zu laufenden Projekten wenden Sie sich gerne an:
Im Rahmen der Kooperation mit dem Institut für Medizinische Informatik nimmt Herr Lukas Niekrenz die Position des Arztes als Bindeglied zwischen Krankenversorgung und Medizinsicher Informatik wahr. Schwerpunkt der Tätigkeit ist es, einen Wissenstransfer zwischen den Medizinischen Kliniken I und V und dem Institut für Medizinische Informatik aufzubauen, sowie die Erkenntnisse aus den Forschungsprojekten in die klinische Routine zu überführen. Dies umfasst z. B. Projekte, bei denen Routinedaten für die Forschung bereitgestellt werden oder bei denen Entscheidungen und Prozesse in der Klinik durch IT-Systeme unterstützt und verbessert werden sollen. Das Ziel der Kooperation ist die Digitalisierung in der Pneumologie, Kardiologie und internistischen Intensivmedizin zu gestalten und voranzutreiben.
Konkret beteiligt sich die Klinik für Pneumologie und Internistische Intensivmedizin so zum Beispiel im Rahmen des egePan Unimed Verbundprojekts des Netzwerkes Universitätsmedizin an der „COVID-19@Home“-Studie, die einen Beitrag zur Forschung zur Pandemiebewältigung leisten soll.
Im Rahmen dieses Projekts zur telemedizinischen Unterstützung von ambulant behandelten COVID-19-Patientinnen und Patienten erhalten diese Messgeräte mit Smartphoneschnittstelle zur Dokumentation ihres Gesundheitszustandes während der Infektion. Dieses digitale Gesundheitstagebuch liefert wertvolle Informationen, die die ärztliche Behandlung der Patientinnen und Patienten unterstützen sollen.
Mit den gewonnenen Daten und der Kombination aus qualitativen und quantitativen Erhebungen werden Empfehlungen für das Behandlungsmanagement von COVID-19-Patientinnen und Patienten sowie Transferkonzepte erarbeitet.
Das Projekt wird in enger Zusammenarbeit mit der Zentralen Notaufnahme durchgeführt.
Kontakt und Informationen
Lukas Niekrenz
Tel.: 0241 80-37177
lniekrenzukaachende
Die Klinik für Pneumologie und Internistische Intensivmedizin (Medizinische Klinik V) beteiligt sich an der im Folgenden aufgeführten COVAS Studie. Dabei sind bereits jetzt mehrere Publikationen aus dieser Beteiligung entstanden, die hier einsehbar sind.
Eine nähere Beschreibung dieses fächerübergreifenden COVID-19 Forschungsprojektes der Uniklinik RWTH Aachen ist folgender Homepage zu entnehmen:
www.cbmb.rwth-aachen.de/register_studien/covas-studie/
CAPNETZ Studie
Kompetenznetzwerk „Ambulant erworbene Pneumonie“ – Beobachtungsstudie, die die Verbesserung der Versorgung von Patienten mit ambulant erworbener Pneumonie zum Ziel hat.
www.capnetz.de/html/patients/flyer/flyer1213
Kontakt und Information:
Gaby Heuer
Tel.: 0241 80-35881
gheuerukaachende