Forschungsprojekte
Aktuell
BMBF: VR-VTK - Virtual Reality in der Versuchstierkunde
- Verantwortliche Wissenschaftler:
- PD Dr. Christian Bleilevens
- Virtuelle Realität bietet die Möglichkeit nahezu alle Methoden und Handgriffe die in der tierexperimentellen Grundausbildung erforderlich sind realitätsnah darzustellen. Die Durchführung vieler Methoden lassen sich auf diese Weise komplett ersetzen, andere lassen sich vor der Eigentlichen Durchführung optimal trainieren – Die Tierzahl Reduktion und Verfeinerung der Methodik im Sinne der 3R (Reduction, Replacement, Refinement) wird auf diese Weise vorangetrieben.

DFG SPP2014: „Towards Implantable Lungs“
- Projekt: “NO-releasing and DNase labeled Microgels as new antithrombogenic coating for Membrane lungs”
- Verantwortliche Wissenschaftler:
- Univ.- Prof. Dr. med. Rolf Rossaint
- PD Dr. Christian Bleilevens
- Verantwortliche Wissenschaftler:
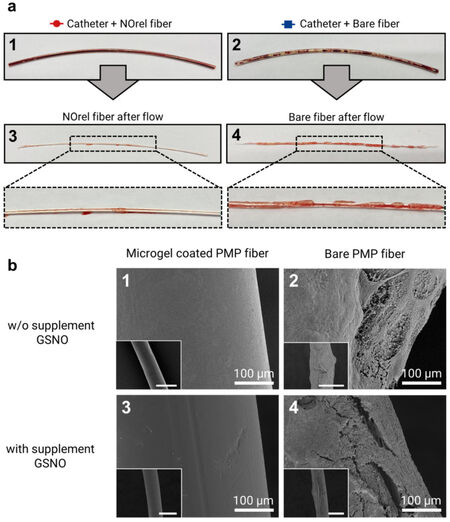
- In diesem Gemeinschaftsprojekt mit dem „DWI- Leibnitz Institut für interaktive Materialien“ und der Klinik für Anästhesiologie der Uniklinik Münster, wird eine neuartige und sich selbst erneuernde, antithrombogene Beschichtung für Poly-Methyl-Penten (PMP) Fasern in Oxygenatoren entwickelt. Microgele imitieren die Enzymfunktion der Glutathion-Peroxidase, die aus natürlichen Quellen für Stickstoffmonoxid (NO) im Körper z.B. S-Nitrosoalbumin, NO abspalten kann. NO vermindert u.a. die Thrombozytenaktivierung und so entstehen lokal auf der PMP Membran weniger Thromben. In Kombination mit DNase besetzen Microgelen, werden Neutrophile-Extrazelluläre-Fallen (NETs, kondensierte DNA-Fäden) durch den Verdau der DNA-Fäden reduziert und die Stabilität potentiell entstehender Thromben dadurch deutlich verringert.
- Publikationen:
- Endogenous Nitric Oxide-Releasing Microgel Coating Prevents Clot Formation on Oxygenator Fibers Exposed to In Vitro Blood Flow - PubMed (nih.gov)
- DNase I functional microgels for neutrophil extracellular trap disruption - PubMed (nih.gov)
- Bioactive Nanogels Mimicking the Antithrombogenic Nitric Oxide-Release Function of the Endothelium - PubMed (nih.gov)
- Publikationen:
DFG: Die Rolle des Makrophagen Migrationsinhibierender Faktor (MIF) nach Myokardinfarkt im Mausmodell
- Verantwortliche Wissenschaftler:
- PD Dr. Christian Bleilevens
- Prof. Dr. med. Christian Stoppe (Uniklinikum Würzburg)
- Dr. rer. nat. Josefin Soppert
- Herzkreislauferkrankungen, speziell der Myokardinfarkt, gehören zu den häufigsten Todesursachen weltweit und die Standardtherapie eines Herzinfarktes ist eine rasche Wiederherstellung der Durchblutung der verschlossenen Herzkranzgefäße (Reperfusion). Jedoch führt die erneute Durchblutung des zuvor minderdurchbluteten Herzmuskels zu einer zusätzlichen Schädigung. Die Abfolge von Ischämie und Reperfusion (I/R) führt zu einem vermehrten Sterben der Herzmuskelzellen, unmittelbar gefolgt von einer starken Entzündungsreaktion. Das Ausmaß des Zellsterbens und die daraus resultierende Infarktgröße ist nach wie vor ein wichtiger Indikator für das Outcome und steht in direktem Zusammenhang mit der Gesamtmortalität sowie der Hospitalisierung im Falle einer resultierenden Herzinsuffizienz nach einem Infarkt. Viele verschiedene Arten des programmierten Zelltods (Nekroptose, Pyroptose, Ferroptose, Parthanatos) scheinen eine wichtige Rolle bei dem Krankheitsverlauf des reperfundierten Myokardinfarkts zu spielen. Das Zytokin Makrophagen Migrationsinhibierender Faktor (MIF) ist in (fast) allen programmierten Zelltod-Formen involviert und stellt aufgrund seiner einerseits kardioprotektiven als auch entzündungsfördernden Eigenschaften sowie seiner Rolle in der Regulation der Zelltod-Formen ein interessantes therapeutisches Ziel dar. Ein möglicher Modulator von MIF könnte sein löslicher Rezeptor CD74 (sCD74) sein, dessen Einfluss auf MIF und die resultierende Regulation der Zelltod-Formen nach Myokardinfarkt gänzlich unerforscht sind. Daher wird die Rolle von MIF sowie der regulatorische Einfluss von sCD74 auf MIF in der Zelltod-Regulation nach einem induzierten einstündigen Myokardinfarkt und anschließender Reperfusion in Wildtyp-Mäusen sowie Mäusen die kein MIF Protein herstellen können (MIF knockout) untersucht. Die iterative Gabe von sCD74 oder PBS als Kontrolle, zu verschiedenen Zeitpunkten während des Prozesses, soll das Potenzial von sCD74 als möglichen therapeutischen Modulator aufklären.
START Projekt: Faserbasierte Bioimpedanzmessung von Blut zur Echtzeitüberwachung der Thrombenbildung an Oxygenatormembranen
- Verantwortliche Wissenschaftler:
- PD Dr. Christian Bleilevens
- Dr. med. Patrick Winnersbach
- Die Gerinnsel-Früherkennung in einem Oxygenator findet nach heutigem Standard immer noch über einen Druckanstieg vor dem Oxygenator statt. Steigt der Druck rasant an, ist es jedoch bereits zu spät – denn ein Blutgerinnsel hat sich gebildet und der Oxygenator muss notfallmäßig gewechselt werden. In diesem Projekt wird im Rahmen einer START-Förderung in Kooperation mit dem Institut für Textiltechnik der RWTH Aachen die Impedanzmessung als Früherkennungssystem im Vergleich zum Goldstandard (Druckmessung) getestet. In einem in vitro Setting konnten mittels Sensorfasern zur Bioimpedanzmessung bereits Blutgerinnsel in einer Testkammer detektiert werden. Verglichen mit dem klinischen Standard der Druckmessung zeigte sich die Bioimpedanzmessung als zuverlässig und konnte darüber hinaus entstehende Blutgerinnsel signifikant früher detektieren.

- Im Rahmen des START-Projekts „Faserbasierte Bioimpedanzmessung von Blut zur Echtzeitüberwachung der Thrombenbildung an Oxygenatormembranen“ werden die Sensorfasern nun in einen miniaturisierten Oxygenator integriert, um die Echtzeitdetektion der Gerinnselbildung an der Oxygenatormembran via Bioimpedanzmessung zu ermöglichen. Die Integration der Sensorfasern in den Oxygenator erfolgt in Kooperation mit dem Institut für Angewandte Medizintechnik (CVE) der RWTH, welches Expertise in der Konzeption und Herstellung individueller Oxygenatoren besitzt. Die Evaluation erfolgt in einem in vitro Testkreislauf unter Verwendung von Humanblut, sowie im Vergleich zur herkömmlichen Druckmessung, um die Möglichkeiten und Grenzen der Bioimpedanzmessung zur Echtzeitdetektion von Blutgerinnseln, zu ermitteln.
Identifikation, geschlechterdifferenzierte Analyse und Einsatz von Ex Vivo mittels Ratten-ECMO gewonnen Extrazellulären Vesikeln in humanen Kardiomyozyten (Rat[EV]2)
- Verantwortlicher Wissenschaftler:
- Dr. med. Matthias Deininger (OIM)
- PD Dr. Christian Bleilevens (AN)
- Prof. Dr. Thomas Breuer (OIM)
Die extrakorporale Membranoxygenierung (ECMO) wird zunehmend im Rahmen der extrakorporalen kardiopulmonalen Reanimation (eCPR) als „Bridge-to-Recovery“-Verfahren eingesetzt. Eine prolongierte Organunterstützung bei eCPR kann jedoch zu metabolischer und inflammatorischer Dysregulation führen, was eine umfassende, globale und kritische Organversorgung erforderlich macht und eine große intensivmedizinische Herausforderung darstellt.
In diesem Kontext gewinnen extrazelluläre Vesikel (EVs) zunehmend an Bedeutung. Sie werden von nahezu allen Zellen zur interzellulären Kommunikation freigesetzt und gelten als vielversprechende Kandidaten für diagnostische und therapeutische Ansätze. Bislang existieren jedoch keine systematischen Studien zur Freisetzung und Zusammensetzung von EVs unter den Bedingungen einer prolongierten, kritischen Organversorgung wie bei eCPR.
Unsere Arbeitsgruppe hat daher ein post-mortales Ratten-ECMO-Modell etabliert, das einen prolongierten, kritischen Multiorganversorgungszustand unter extremen metabolisch-inflammatorischen Bedingungen nachbildet. Dieses Modell bildet die Grundlage für die systematische Untersuchung von EV-Freisetzung und -Fracht unter lebensbedrohlichen Organstress-Bedingungen.
Ribonuklease als neue therapeutische Zielstruktur in der septischen Kardiomyopathie - experimentelles Sepsis Modell in der Maus
- Verantwortlicher Wissenschaftler:
- PD Dr. med. Lukas Martin (OIM)
- Dr. rer. nat. Sandra Krämer
- Dr. rer. medic. Elisabeth Zechendorf (OIM)
- PD Dr. Christian Bleilevens (AN)
Sepsis ist eine der häufigsten Todesursachen auf Intensivstationen und eng mit dem Auftreten von Multiorganversagen verbunden. Neben der bekannten Lungenbeteiligung rückt zunehmend die septische Kardiomyopathie in den Fokus, eine bisher unzureichend verstandene Komplikation.
Ziel dieses Projekts ist die Etablierung eines standardisierten Mausmodells zur Induktion einer polymikrobiellen Sepsis auf Basis eines zökalen Slurry-Präparats (cecal slurry, CS). Das Modell stellt eine reproduzierbare und weniger belastende Alternative zum klassischen CLP-Modell dar. Hierbei wird der Darminhalt von Spender-Mäusen unter sterilen Bedingungen aufbereitet und intraperitoneal injiziert. Die Tiere werden 24 Stunden lang beobachtet, um Veränderungen der Herzfunktion mittels Echokardiographie sowie biochemische und histologische Marker zu analysieren. Dazu zählen Herzapoptose, Troponin I, CK-MB, BNP und pro- sowie antiinflammatorische Zytokine wie IL-6, IL-10 und TNF. Geschlechtsspezifische Unterschiede werden ebenfalls untersucht.
Im zweiten Teil des Projekts wird die therapeutische Wirkung von RNase 1 getestet. Dieses endogene antimikrobielle Peptid besitzt immunmodulatorische und zellprotektive Eigenschaften. Die Auswertung erfolgt anhand derselben funktionellen, biochemischen und histologischen Parameter wie im ersten Versuchsteil, einschließlich geschlechtsspezifischer Analysen.
Dieses Projekt trägt dazu bei, Mechanismen der septischen Kardiomyopathie besser zu verstehen und die Wirksamkeit potenzieller Therapien unter realistischen experimentellen Bedingungen zu evaluieren.
Geplant
Virtual Reality (VR) and Augmented Reality (AR) in Medical Education – New Perspectives for Students and Innovative Teaching Methods for Educators
- Verantwortlicher Wissenschaftler:
- PD Dr. Christian Bleilevens (AN)
- Martin Lemos (AVMZ)
- Prof. Dr. Thomas Breuer (OIM)
Die COVID-19-Pandemie hat die digitale Transformation der deutschen medizinischen Fakultäten deutlich beschleunigt. Lehrpläne mussten rasch auf digitale Plattformen angepasst werden, um die Qualität von Lehre und Ausbildung aufrechtzuerhalten. Neben etablierten Videokonferenzlösungen gewinnen Virtual Reality (VR) und Augmented Reality (AR) zunehmend an Bedeutung. Diese Technologien ermöglichen praxisnahes Lernen, reduzieren die Abhängigkeit von erfahrenen Lehrkräften vor Ort und schaffen sichere Übungsumgebungen.
Traditionelle medizinische Ausbildung beruht stark auf Präsenzunterricht, praktischen Übungen und Mentoring. Faktoren wie begrenzte Verfügbarkeit von Ausbildern, Patientensicherheit und Ressourcenknappheit schränken jedoch oft die Ausbildungsmöglichkeiten ein. VR und AR bieten hier Lösungen: Studierende können komplexe Verfahren interaktiv und standardisiert in kontrollierten virtuellen Umgebungen trainieren. Immersive VR erzeugt das Gefühl physischer Präsenz im virtuellen Raum und fördert kognitive, psychomotorische und soziale Fähigkeiten. AR erweitert die reale Umgebung um computergenerierte Inhalte und bereichert so den Lernprozess.
Eine aktuelle systematische Übersichtsarbeit von Tene et al. analysierte 28 Studien zu VR und AR in der medizinischen Ausbildung. Die Ergebnisse zeigen positive Effekte auf die Kompetenzen der Studierenden, wenngleich statistische Signifikanz noch nicht erreicht wurde. Dies unterstreicht das Potenzial immersiver Technologien und den Bedarf an weiterer Forschung.
Darüber hinaus integriert Extended Reality (XR) digitale und reale Lerninhalte, wodurch theoretisches Wissen und klinische Praxis verbunden werden können. Die Verschmelzung digitaler Overlays mit realen Patientenkontakten könnte die klinische Ausbildung, chirurgische Planung und interdisziplinäre Zusammenarbeit revolutionieren. Angesichts des steigenden globalen Bedarfs an medizinischem Personal und prognostizierter Ärztemangel wird der Einsatz immersiver Technologien für eine hochwertige, skalierbare und personalisierte medizinische Ausbildung zunehmend entscheidend.
Abgeschlossen
BMBF: Alternativen zum Tierversuch “AutoMock”
- Verantwortliche Wissenschaftler:
- PD Dr. Christian Bleilevens
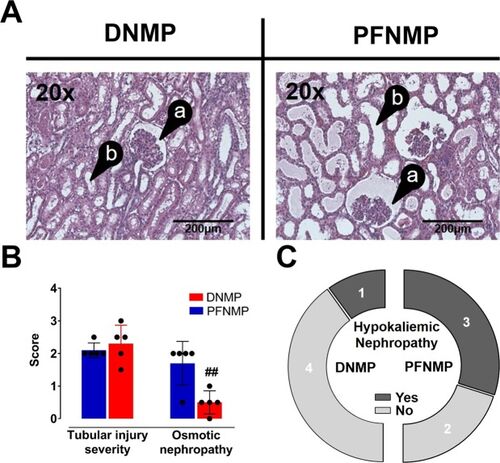
- In diesem Projekt konnte erfolgreich ein voll automatisierte Perfusionsstand für Schweinenieren entwickelt werden, mit dessen Hilfe die Nieren aus insgesamt 35 Hausschweinen, die am UKA in anderen AGs verwendet wurden, und so wissenschaftliche Fragestellungen beantwortet werden konnten, ohne zusätzliche Tiere zu verwenden. Dies entspricht einer Einsparung von >20% der Versuchstiere, welche in Deutschland im Jahresdurchschnitt für die Erforschung neuer Nierenperfusionsstrategien verwendet werden. Der teststand reguliert seinen Perfusionsdruck, den pH Wert der Perfusats, sowie den Füllstand autonom über ein CAN-BUS basiertes Netzwerk, dass von den Kooperationspartner der Informatik11 „Embedded Software“ entwickelt wurde. Es könne 6 Std. normotherme Maschinenperfusion erreicht werden. Ziel ist es, ein klinisch verwendbares, normothermes Perfusionssystem weiterzuentwickeln.
- Publikationen:
- Cold Preflush of Porcine Kidney Grafts Prior to Normothermic Machine Perfusion Aggravates Ischemia Reperfusion Injury - PubMed (nih.gov)
- Influence of Vitamin C on Antioxidant Capacity of In Vitro Perfused Porcine Kidneys - PubMed (nih.gov)
- HBOC-301 in Porcine Kidney Normothermic Machine Perfusion and the Effect of Vitamin C on Methemoglobin Formation - PubMed (nih.gov)
- Taurine as Antioxidant in a Novel Cell- and Oxygen Carrier-Free Perfusate for Normothermic Machine Perfusion of Porcine Kidneys - PubMed (nih.gov)
- Doktorarbeit: Eine weitere Arbeit in Vorbereitung zur Publikation die den Vergleich komplett Zellfreiem Perfusat für Nieren mit dem Goldstandard (Erythrozytenkonzentrate + Puffer) vergleicht.
- Bachelor- und Master-Abschlussarbeiten am Institut für Embedded Software (Informatik 11) Neuigkeiten [Informatik 11 - Embedded Software] (rwth-aachen.de)
- Publikationen:
EIT Projekte: in vitro Testkreisläufe für Herzunterstützungssysteme
- Verantwortliche Wissenschaftler:
- PD Dr. Christian Bleilevens
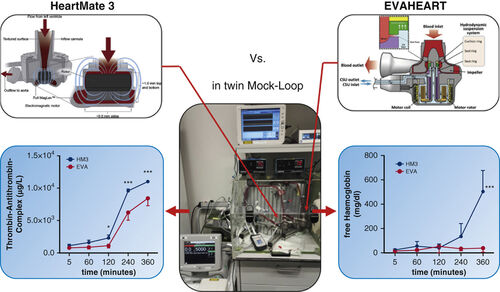
- Aus diesem Projekt resultieren die für die aktuellen Projekte genutzten Testkreisläufe, die zum Ziel hatten, möglichst klinikrelevant medizinische Produkte zu testen (Verwendung von Humanblut, Einhaltung relevanter Blut-Drücke, -Flüsse und -Temperaturen). Wichtig bei der Verwendung von Humanblut ist ein realistisches Füllvolumen zu schaffen, da Humanblut nur in äußerst begrenzter Menge zur Verfügung steht. Als Weiterentwicklung vorangegangener, größerer Testkreisläufe für Tierblut, werden für aktuelle Studien die teststände für Humanblut genutzt.
- Publikationen:
- In vitro comparison of the hemocompatibility of two centrifugal left ventricular assist devices - PubMed (nih.gov)
- In vitro head-to-head comparison of anticoagulation properties of two heparin brands in a human blood miniature mock loop - PubMed (nih.gov)
- Septic porcine blood does not further activate coagulation during in vitro membrane oxygenation - PubMed (nih.gov)
- Twelve Hours In Vitro Biocompatibility Testing of Membrane Oxygenators - PubMed (nih.gov)
- Publikationen:
START Projekte etc.
- Verantwortliche Wissenschaftler:
- PD Dr. Christian Bleilevens
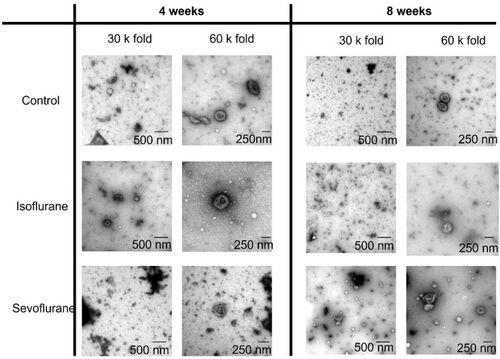
- Die Tierexperimentellen Versuche haben i.d.R. die organprotektive Wirkung verschiedener Anästhetika in verschiedenen Schädigungsmodellen, oder klinischen Szenarien im Fokus. Beispielswiese ist die Anästhetische Prä- oder auch Postkonditionierung bekannt für ihren Einfluss auf verschiedene Organsysteme, die dann einer Ischämie oder sonstigen Schädigung ausgesetzt werden. Zahlreiche Mechanismen liegen dieser Wirkung zugrunde, beispielswiese die Formation extrazellulärer Vesikel nach Präkonditionierung, wie systematisch in vitro und in vivo untersucht wurde. Ein anders Beispiel ist das Schlaganfallmodell in der Ratte, in dem neuroprotektive Effekte unterschiedlicher Medikamente getestet werden können.
- Publikationen:
- Repetitive Treatment with Volatile Anesthetics Does Not Affect the In Vivo Plasma Concentration and Composition of Extracellular Vesicles in Rats - PubMed (nih.gov)
- Evaluation of the cardioprotective potential of extracellular vesicles - a systematic review and meta-analysis - PubMed (nih.gov)
- Insular infarct size but not levosimendan influenced myocardial injury triggered by cerebral ischemia in rats - PubMed (nih.gov)
- Publikationen: