Bak Group
Translationale Neurophysiologie und Modellierung neurologischer Erkrankungen im menschlichen Gehirn
Die translational ausgerichtete Neurophysiologie widmet sich der Erforschung physiologischer und pathologischer Prozesse im menschlichen Gehirn mit dem Ziel, daraus gewonnene Erkenntnisse in die Verbesserung von Diagnose, Therapie und Prävention neurologischer Erkrankungen zu gewinnen. Ein zentraler Aspekt dieser Arbeit ist die Nutzung humaner experimenteller Systeme, da tierexperimentelle Modelle trotz ihres wissenschaftlichen Werts in ihrer Übertragbarkeit auf den Menschen oft limitiert sind.
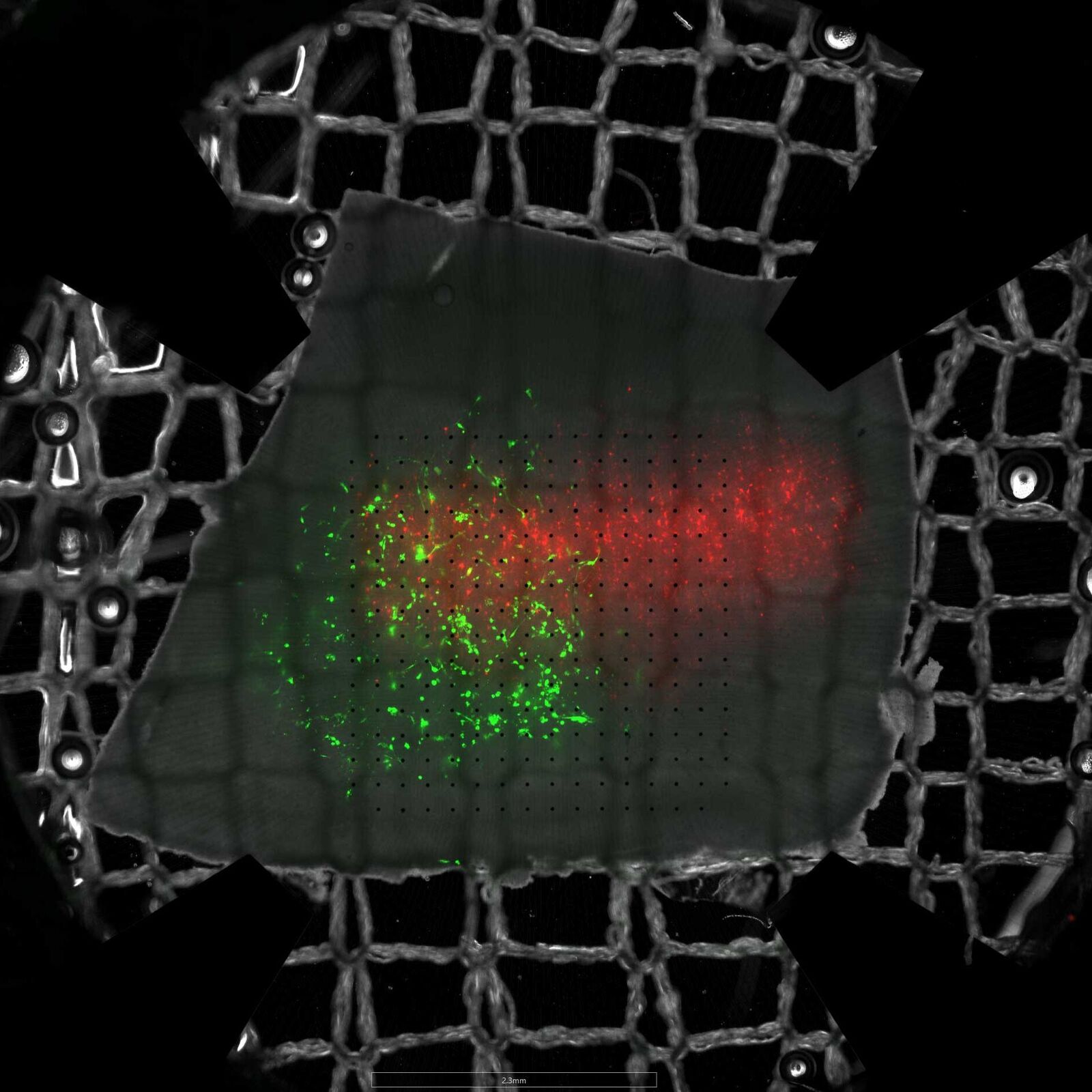
Im Fokus steht die Arbeit mit organotypischen Hirnschnittkulturen aus menschlichem Hirngewebe, die es ermöglichen, neuronale Netzwerke in gesundem wie auch pathologischem Zustand unter möglichst natürlichen Bedingungen zu untersuchen. Dieses Modell erlaubt detaillierte Einblicke in krankheitsspezifische Mechanismen direkt im menschlichen Kontext und bietet eine vielversprechende Grundlage für die Entwicklung und Testung therapeutischer Ansätze.
Unser übergeordnetes Ziel ist es, die Lücke zwischen experimenteller Neurowissenschaft und klinischer Anwendung zu schließen – durch den Einsatz reduktionistischer, jedoch translational relevanter Modellplattformen, die ethisch verantwortungsvoll sind und eine zukunftsorientierte Forschung am Menschen ermöglichen.

Aniella Bak
abakukaachende
Address
Dept. of Neurology, Section Epileptology
University of Aachen
Pauwelsstrasse 30
52074 Aachen, Germany
Tel. +49-(0)241 80-38786

Birgit Gittel (lead technician)
bgittelukaachende
Address
Dept. of Neurology, Section Epileptology
University of Aachen
Pauwelsstrasse 30
52074 Aachen, Germany
Tel. +49-(0)241-80-38611

Carina Haaken
chaakenukaachende
Address
Dept. of Neurology, Section Epileptology
University of Aachen
Pauwelsstrasse 30
52074 Aachen, Germany
Organotypische Hirnschnittkulturen können aus Maus- oder menschlichem Hirngewebe präpariert werden und erhalten die dreidimensionale Architektur der ursprünglichen Hirnregion, einschließlich der nativen Zelltypen, ihrer Interaktionen sowie des genetischen und molekularen Hintergrunds des Gewebespenders. Diese Kulturen können über mehrere Wochen in vitro erhalten bleiben und eröffnen damit ein einzigartiges Zeitfenster für langfristige Beobachtung, Manipulation und Analyse. Besonders menschliches Hirngewebe ist sehr empfindlich, weshalb wir kontinuierlich daran arbeiten, unsere Protokolle zu optimieren und die Lebensfähigkeit und Qualität der Kulturen zu verbessern. Darüber hinaus charakterisieren wir systematisch, wie sich das Gewebe in vitro anpasst, verhält und über die Zeit verändert.
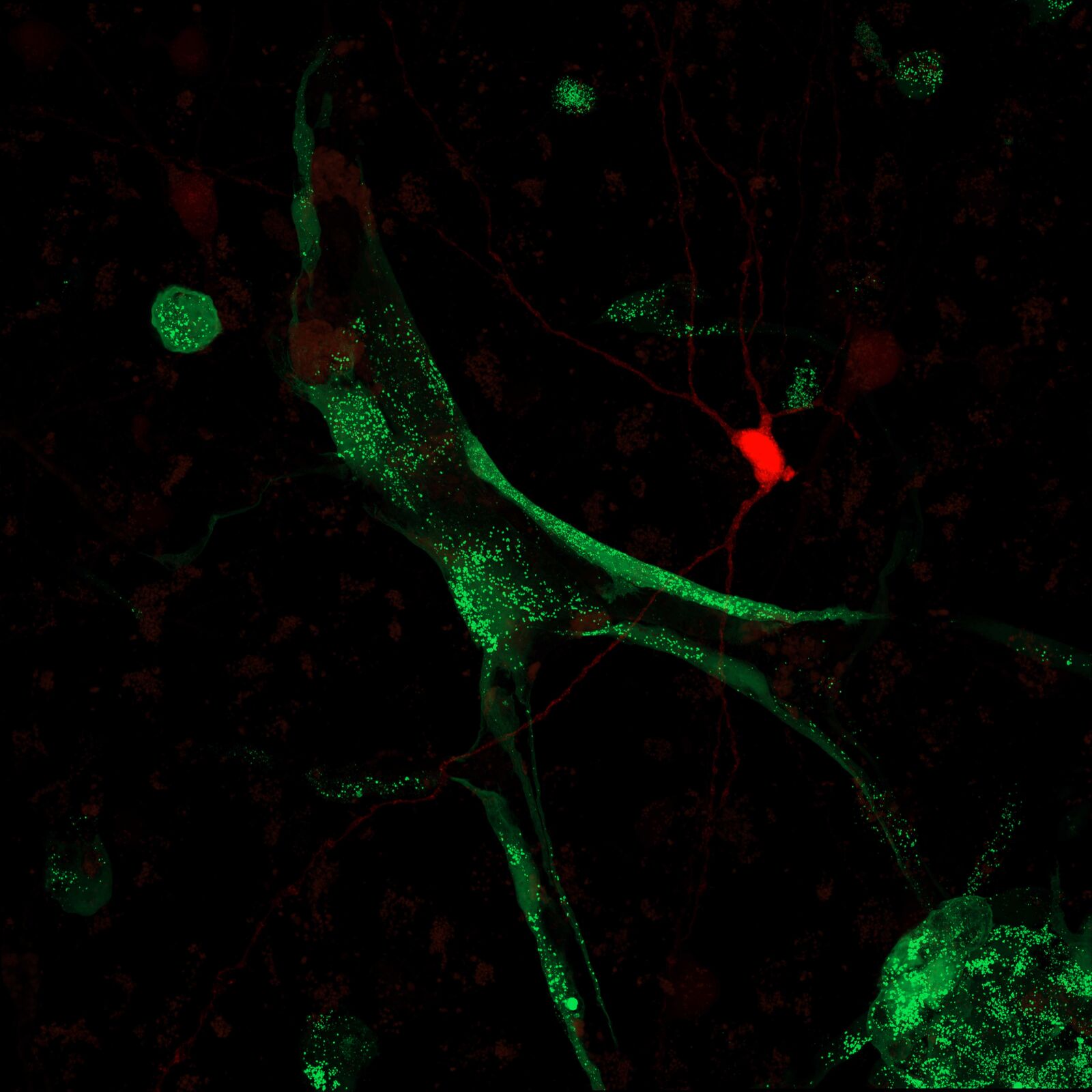
Das Glioblastom ist ein besonders aggressiver und verheerender Hirntumor mit äußerst schlechter Prognose für die Betroffenen. Obwohl bereits zahlreiche Studien zur Pathogenese, Progression und Behandlung des Glioblastoms in Tiermodellen durchgeführt wurden, sind Untersuchungen am menschlichen Gewebe unerlässlich, um eine verbesserte Übertragbarkeit auf den Mensch zu ermöglichen. Wir haben ein Ko-Kulturmodell aus primären, patientenabgeleiteten Glioblastomzellen und menschlichem Kortexgewebe etabliert, das es uns erlaubt, die Interaktion zwischen Tumorzellen und dem endogenen menschlichen neuronalen Netzwerk auf elektrophysiologischer, molekularer und transkriptomischer Ebene zu untersuchen.
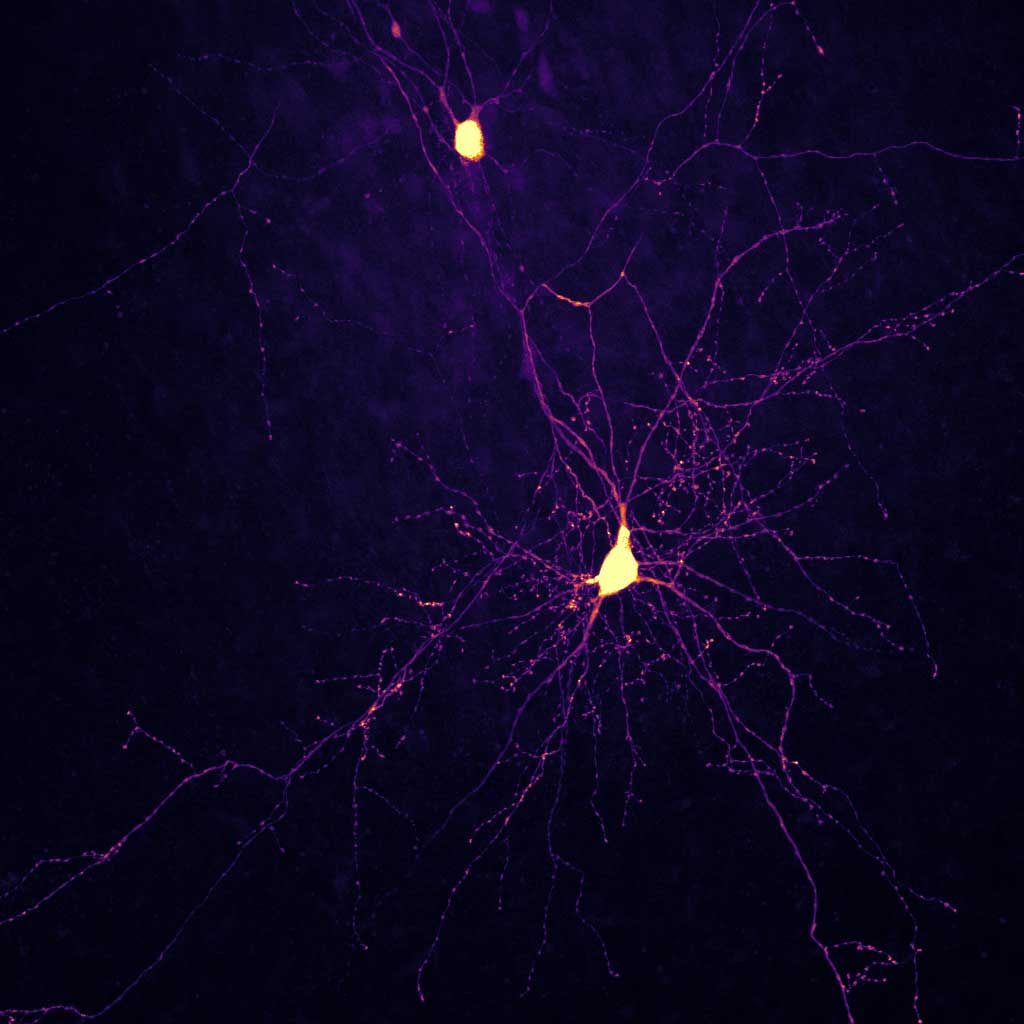
Epilepsie ist eine chronische neurologische Erkrankung, die durch wiederkehrende, nicht provozierte Anfälle gekennzeichnet ist und weltweit etwa 50 Millionen Menschen betrifft. Die Ursachen sind vielfältig und umfassen genetische Mutationen, Hirnverletzungen, Entwicklungsstörungen und Infektionen. Mutationen in Genen, die zuvor nicht mit Epilepsie in Verbindung gebracht wurden – sogenannte „Epilepsie-Kandidatengene“ – werden zunehmend als mögliche Auslöser identifiziert. In unseren Hirnschnittkulturen können wir sowohl genetisch bedingte Epilepsien, zum Beispiel durch Knockdown eines Epilepsie-Kandidatengens, als auch erworbene Epilepsien, etwa infolge einer Hirnverletzung, modellieren. Dieses System ermöglicht es uns, die Epileptogenese zu untersuchen, den resultierenden Phänotyp und die zugrunde liegenden molekularen Dysfunktionen zu charakterisieren und nach neuen potenziellen Therapieansätzen zu suchen.
Yang, D., Qi, G., Ort, J., Witzig, V., Bak, A., Delev, D., Koch, H., & Feldmeyer, D. (2024). Modulation of large rhythmic depolarizations in human large basket cells by norepinephrine and acetylcholine. Communications Biology, 7, 885. https://doi.org/10.1038/s42003-024-06546-2
Bak, A., Koch, H., van Loo, K. M. J., Schmied, K., Gittel, B., Weber, Y., Ort, J., Schwarz, N., Tauber, S. C., Wuttke, T. V., & Delev, D. (2023). Human organotypic brain slice cultures: A detailed and improved protocol for preparation and long-term maintenance. Journal of Neuroscience Methods, 404, 110055. https://doi.org/10.1016/j.jneumeth.2023.110055
This paper was honored with the “Paper of the Quarter” award for the first quarter of 2024 from the 3R competence network NRW.
Bak, A., Schmied, K., Jakob, M. L., Bedogni, F., Squire, O. A., Gittel, B., Jesinghausen, M., Schünemann, K. D., Weber, Y., Kampa, B., van Loo, K. M. J., & Koch, H. (2024). Temporal dynamics of neocortical development in organotypic mouse brain cultures: A comprehensive analysis. Journal of Neurophysiology, 132(3). https://doi.org/10.1152/jn.00178.2024
Qi, G., Yang, D., Bak, A., Hucko, W., Delev, D., Hamou, H., Feldmeyer, D., & Koch, H. (2024). Transport-related effects on intrinsic and synaptic properties of human cortical neurons: A comparative study. bioRxiv. https://doi.org/10.1101/2024.10.30.621044
Schünemann, K. D., Hattingh, R. M., Verhoog, M. B., Yang, D., Bak, A. V., Peter, S., van Loo, K. M. J., Wolking, S., Kronenberg-Versteeg, D., Weber, Y., Schwarz, N., Raimondo, J. V., Melvill, R., Tromp, S. A., Butler, J. T., Höllig, A., Delev, D., Wuttke, T. V., Kampa, B. M., & Koch, H. (2025). Comprehensive analysis of human dendritic spine morphology and density. Journal of Neurophysiology, 133(4), 1086–1102. https://doi.org/10.1152/jn.00622.2024
Jütten, K., Ort, J., Kernbach, J. M., Meyer-Baese, A., Meyer-Baese, U., Hamou, H. A., Clusmann, H., Wiesmann, M., Bremer, J., Koch, H., Bak, A., Ricklefs, F., Drexler, R., Heiland, D.-H., & Delev, D. (2025). High peritumoral network connectedness in glioblastoma reveals a distinct epigenetic signature and is associated with decreased overall survival. Neuro-Oncology. Advance online publication. https://doi.org/10.1093/neuonc/noaf101





