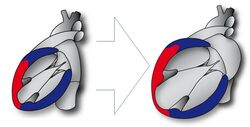
Kardiales Remodeling
Nachdem sich unsere Arbeitsgruppe mit dem kardialen Remodeling nach Myokardinfarkt bzw. Ischämie-Reperfusionsschaden beschäftigt hat, stehen jetzt die Effekte einer Aortenstenose und Lebererkrankung im Fokus. Dabei nutzen wir in den verschiedenen Modellen die etablierten Methoden zur Analyse der Funktion und Perfusion, sowie die histologische und molekularbiologische Beschreibung struktureller Veränderungen.
Aktuelle Projekte
Eine akute und chronische Lebererkrankung kann die kardiale Funktion über verschiedene Mechanismen entscheidend beeinträchtigen. So führt eine Leberzirrhose nach längerer Zeit zu einer sogenannten zirrhotischen Kardiomyopathie, dessen Pathomechanismus noch nicht genau geklärt ist. Nach einer initialen konzentrischen Hypertrophie, Hyperkontraktilität in Ruhe und daraus folgend einer reduzierten kontraktilen Reserve zeigt sich später eine exzentrische Hypertrophie mit einer eingeschränkten Funktion in Ruhe. Bereits eine subklinische kardiale Funktionsstörung in Ruhe, die sich mittels Strain-Analyse darstellen lässt, ist ein unabhängiger Prädiktor für die Sterblichkeit bei Kandidaten für eine Lebertransplantation.
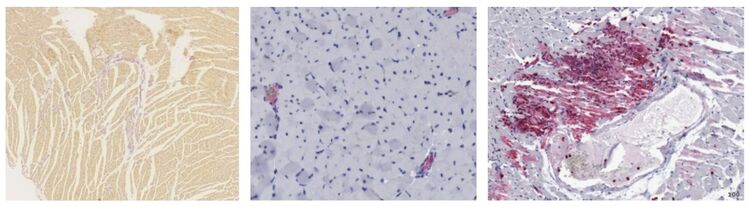
Weit weniger bekannt ist die kardiale Schädigung in Folge eines akuten Leberschadens. Sowohl klinisch, als auch experimentell lassen sich ein diffuser Myokardschaden als Ursache einer erhöhten Sterblichkeit nachweisen. Die Ursache könnte hier in der Störung der Mikrozirkulation liegen, da sich sowohl perivaskuläre Läsionen, als auch Mikrothromben nachweisen lassen (siehe Abbildung).
Mitarbeiter
- Marc Hein, Mare Mechelinck, Moritz Uhlig
Die Grenzen bei denen eine Aortenstenose in Narkose dekompensiert sind kaum vorhersagbar und die Mechanismen nicht eindeutig geklärt. Bisherige experimentelle Modelle können die Pathophysiologie nur bedingt abbilden, da oft nur eine supravalvuläre Stenose induziert werden kann (TAC). Daher kombinieren wir das TAC-Modell mit der Induktion einer koronaren Stenose. Weiterhin wird die Methode genutzt, um die molekulargenetischen Veränderungen im Rahmen des adversen Remodelings bei Aortenstenose zu untersuchen und neue therapeutische Targets zu identifizieren.
Mitarbeiter
- Marc Hein, Moritz Uhlig, David Schumacher