Aplastische Anämie, Paroxysmale Nächtliche Hämoglobinurie und Bone Marrow Failure Syndromes („Knochenmarkversagen-Syndrome“, BMFS)
Sehr geehrte Besucherin, sehr geehrter Besucher,
herzlich Willkommen in der Klinik für Hämatologie, Onkologie, Hämostaseologie und Stammzelltransplantation (Med. Klinik IV) der Uniklinik RWTH Aachen.
Ein Schwerpunkt unserer Klinik liegt in der Diagnose und Behandlung so genannter Knochenmarkversagen-Erkrankungen (englisch: bone marrow failure syndromes, BMFS). Hierzu gehören Erkrankungen wie die Aplastische Anämie, die Paroxysmale nächtliche Hämoglobinurie (PNH) und weitere, meist angeborene Formen von Knochenmarkversagen-Erkrankungen. Wir bieten im Rahmen unserer Spezialsprechstunden umfangreiche Informationen, modernste Diagnostik und eine patientenorientierte Beratung für Patienten mit BMFS, einschließlich Telomeropathien, an. Darüber hinaus besteht häufig die Möglichkeit zur Teilnahme an klinischen Studien. Letztere bieten hierbei das Potential neuste Therapieformen noch vor finaler Zulassung zu erhalten. So kann im Rahmen von Studien beispielsweise aus einer ursprünglich regelmäßigen Therapie über die Vene eine Tablettentherapie werden oder ein neues Medikament die langfristige Prognose einer Erkrankung deutlich verbessern.
Unser umfassendes Angebot steht im Dienste des Patienten und der weiteren Erforschung und Verbesserung von Versorgungs- und Therapiemöglichkeiten.
Für Informationen und Rückfragen stehen Ihnen wir und unser Team gerne zur Verfügung.
Herzliche Grüße
Ihr PD Dr. Fabian Beier, PD Dr. Jens Panse und Univ.-Prof. Dr. Tim Brümmendorf
Die Aplastische Anämie ist eine Erkrankung, bei der das Knochenmark zu wenig Blutzellen bildet. Als Folge der verminderten Blutbildung sind mindestens zwei oder drei Arten von Blutzellen in deutlich verringerter Zahl vorhanden. Diese verschiedenen Blutzellarten sind die Blutplättchen (Thrombozyten), die roten Blutkörperchen (Erythrozyten) und die weißen Blutkörperchen (Leukozyten, insbesondere die Granulozyten).
Typische Symptome der Aplastischen Anämie entstehen durch die fehlenden Blutzellen: Ein Mangel an roten Blutkörperchen führt zu einer Blutarmut (Anämie), die mit Müdigkeit, Blässe, Schwäche und Kurzatmigkeit oder Kopfschmerzen bei Anstrengung verbunden ist. Ein Mangel an Blutplättchen (Thrombopenie) führt häufig zu Nasen- oder Zahnfleischblutungen und bei einer starken Verminderung zu kleinen punktförmigen Einblutungen in der Haut und Schleimhaut (Petechien). Ein Mangel an weißen Blutkörperchen (Leukopenie) kann von leichten Infekten, mit oder ohne Fieber, bis hin zu schwersten lebensbedrohlichen Infektionen führen. Dabei sind Infektionen mit Erregern, die bei Menschen mit ausreichend Leukozyten typischerweise nicht vorkommen, wie bspw. Pilzinfektionen, nicht selten. Da bei der Aplastischen Anämie häufig zwei oder drei Arten von Blutzellen fehlen oder vermindert sind, können die Symptome in Kombinationen auftreten.
Die Ursache der Aplastischen Anämie ist häufig ein autoimmuner (also durch das eigene Immunsystem vermittelter) Prozess gegen die blutbildenden Stammzellen. Die Stammzellen werden dabei von körpereigenen Abwehrzellen (so genannten T-Lymphozyten) angegriffen und können in der Folge kein Blut mehr produzieren. Daraus resultieren die oben beschriebenen Verminderungen der Blutzellen und die entsprechenden Beschwerden. Die genaue Ursache des Autoimmunprozesses ist bisher nicht vollständig aufgeklärt.
Die Aplastische Anämie betrifft gehäuft Menschen im jugendlichen Alter oder im höheren Alter ab 45 bis 60 Jahre. Generell kann sie aber in jedem Lebensalter auftreten. Die Diagnose einer Aplastischen Anämie erfordert den Ausschluss anderer Knochenmark-Erkrankungen und wird u. a. mithilfe einer Knochenmarkpunktion gestellt. Man unterteilt die Aplastische Anämie in drei Schweregrade:
- Moderate Aplastische Anämie (auch nicht schwere Aplastische Anämie genannt)
- Schwere Aplastische Anämie
- Sehr schwere Aplastische Anämie
Bei Patienten mit schwerer und sehr schwerer Aplastischer Anämie muss nach Diagnosestellung rasch mit einer Therapie begonnen werden. Grundsätzlich werden zwei Therapieansätze verfolgt: Zum einen eine Erneuerung der blutbildenden Stammzellen durch eine Stammzell-/ Knochenmarktransplantation, zum anderen eine Therapie, die als Ziel hat den Autoimmunprozess zu unterdrücken und den blutbildenden Stammzellen eine Regeneration zu ermöglichen. Diese Therapie nennt man immunsuppressive Therapie (IST).
Für eine Knochenmarktransplantation kommt bei Patienten mit Aplastischer Anämie ein Familien- oder Fremdspender infrage. Je jünger Patienten sind, desto eher wird eine Knochenmarktransplantation angestrebt. Eine immunsuppressive Therapie gegen den zugrunde liegenden Autoimmunangriff wird häufig mit Medikamenten wie Cyclosporin A (CSA) und Antithymozytenglobulin (ATG) durchgeführt. Nach einer IST dauert es meist mehrere Monate bis sich das Knochenmark erholt und es zu einer (manchmal nicht vollständigen) Erholung bzw. Normalisierung der Blutwerte kommt.
Der Verlauf und die Prognose der Aplastischen Anämie konnten in den letzten Jahren deutlich verbessert werden. Mithilfe einer Stammzelltransplantation oder einer immunsuppressiven Therapie kann bei dem größten Teil der Patienten eine verbesserte oder sogar normale Blutbildung erreicht werden. Häufig können die Patienten langfristig wieder ein normales Leben führen.
Die Paroxysmale nächtliche Hämoglobinurie ist eine seltene und unbehandelt potentiell lebensbedrohliche Erkrankung des blutbildenden Systems. Bei der PNH kommt es durch eine plötzliche Mutation in bestimmten Genen zu einem fehlenden Schutz roter Blutkörperchen (Erythrozyten). Dadurch werden die Erythrozyten angreifbar durch das so genannte Komplementsystem. Das Komplementsystem ist ein alter Teil unseres Immunsystems, der kontinuierlich auf der Suche nach körperfremden Eindringlingen ist. Daher existieren in unserem Körper Kontrollmechanismen, die Angriffe gegen körpereigene Strukturen verhindern. Durch die plötzlich neu aufgetretene Genmutation einzelner Stammzellen sind alle aus diesen betroffenen Stammzellen gebildeten Blutzellen nicht mehr vor dem Komplementsystem geschützt. Besonders betroffen sind dabei die roten Blutkörperchen, die zerstört werden und in der Folge Hämoglobin (der rote Blutfarbstoff, in dem wir Eisen speichern) freigesetzt wird.
Die Zerstörung der roten Blutkörperchen und die Freisetzung des Inhaltes der Erythrozyten kann bei Patienten mit PNH eine Vielzahl von Beschwerden verursachen. Häufig leiden Patienten unter einer Blutarmut (Anämie). Diese Anämie zeigt sich durch Symptome wie Müdigkeit, Kurzatmigkeit oder Schwäche. Zusätzlich können Patienten Bauch- und Rückenschmerzen, einen ausgeprägten Erschöpfungszustand (Fatigue) und Gefäßverschlüsse (Thrombosen) entwickeln. Bei Männern kann es darüber hinaus zu Erektionsstörungen kommen. Die namensgebende Dunkelfärbung des Urins durch das freigesetzte Hämoglobin tritt nur bei einem Teil der Patienten auf. Am gefährlichsten sind Thrombosen, die auf Grund der Erkrankung an untypischen Stellen, wie bspw. der Leber, dem Gehirn oder der Haut, auftreten. Die Diagnose einer PNH kann mit einer einfachen Blutabnahme gestellt werden. In speziellen Laboren kann hierzu eine sogenannte Durchflusszytometrie durchgeführt werden, die den Verdacht einer PNH bestätigen kann.
Therapeutisch versucht man bei der PNH die Blutzellen durch eine Blockade des Komplementsystems zu schützen. Diese Blockade erreicht man mit Medikamenten, die über die Vene oder als Injektion ins Unterhautfettgewebe verabreicht werden. In aktuellen Studien finden auch Medikamente in Tablettenform Anwendung. Die Standardbehandlung ist aktuell eine intravenöse Antikörpergabe in achtwöchigen Abständen mit dem Medikament Ravulizumab (Ultomiris®). Durch die Gabe dieser „Komplementinhibitoren“ werden zahlreiche Symptome der PNH gelindert und viele Patienten erfahren eine deutliche Verbesserung ihrer Blutwerte. Die Lebenserwartung der PNH-Patienten entspricht inzwischen der der gesunden Gesamtbevölkerung. Das mit der Therapie verbundene Infektionsrisiko durch Hemmung des Komplementsystems wird durch spezielle Impfungen vermindert.
Die PNH kann eigenständig als „hämolytische PNH“ auftreten oder im Rahmen einer Knochenmarkversagen-Erkrankung in Zusammenhang mit einer Aplastischen Anämie. Daher weisen Patienten neben erniedrigten roten Blutkörperchen manchmal auch eine verminderte Anzahl an weißen Blutkörperchen und Blutplättchen auf. Treten Manifestationen der AA und der PNH zusammen (vereinzelt auch nacheinander) auf, sprechen wir von einem "AA/PNH overlap Syndrom" (Überschneidungssyndrom).
Eine Untergruppe der Aplastischen Syndrome stellen die angeborenen asplastischen Syndrome (englisch: Inherited Bone Marrow Failure Syndrome) dar. Bei ca. 10 % der Patienten mit neu diagnostizierter Aplastischer Anämie wird eine angeborene Ursache für das Fehlen der Blutbildung angenommen. Während bei der erworbenen Aplastischen Anämie die Ursache in einem T-Zell-vermittelten Autoimmunangriff liegt (siehe oben), ist die Ursache für angeborene Aplastische Syndrome eher heterogen. Wie bei der Aplastischen Anämie ist das Fehlen der roten Blutkörperchen (Erythrozyten), Blutplättchen (Thrombozyten) oder weißen Blutkörperchen (Leukozyten), insbesondere der Granulozyten, charakteristisch für die Erkrankung. Im Gegensatz zur erworbenen Aplastischen Anämie findet sich bei den hereditären oder angeborenen Syndromen meist ein genetisch-bedingter, in den blutbildenden Stammzellen liegender Defekt, der zu einer Verminderung der Blutzellen führt.
Dabei lassen sich die angeborenen Syndrome anhand des Alters (Symptombeginn im Kindes- oder Erwachsenenalter) und in Bezug auf die Anzahl der beteiligten Arten von Blutzellen in zwei Gruppen einteilen:
1. Fehlen von einer Blutzellart:
Die Mehrzahl der Erkrankung mit nur einer beteiligten Blutzellart werden häufig im Kindesalter diagnostiziert. Die Gruppe der vererbten aplastischen Syndrome ist vor allem durch das Fehlen der roten Blutkörperchen gekennzeichnet. Fehlende weiße Blutkörperchen (Neutrophile Granulozyten), i.S. einer sogenannten Granulopenie, werden bei der kongenitalen (mit der Geburt erworbenen) Neutropenie (CN) beobachtet. Fehlende rote Blutkörperchen das Diamond Blackfan Syndrom und fehlende Thrombozyten kennzeichnen häufig die sogenannten Thrombocytopenia-absent radius (TAR) Syndrome.
2. Fehlen mehrerer Blutzellarten:
Es existieren auch vererbte Syndrome, die mit einem Fehlen von zwei oder drei Arten von Blutzellen im Sinne einer Bi- oder Panzytopenie einhergehen. Patienten mit diesen Erkrankungen entwickeln manchmal erst im Erwachsenenalter Beschwerden, da die Blutwerte bis dahin nur gering vermindert sein können. Im Erwachsenenalter sind diese vererbten Syndrome mit verminderter Blutbildung diagnostisch oft sehr schwer von einer erworbenen Aplastischen Anämie zu unterscheiden.
Die Hauptvertreter der Gruppe mit einer Beteiligung mehrerer Blutzellarten sind die Fanconi-Anämie, die Telomeropathien (englisch: Telomere biology disorders, TBD) und das Shwachman-Bodian-Diamond-Syndrom.
Durch die sich ständig verbessernde und immer detaillierter werdende Diagnostik der humangenetischen Untersuchungen, ist in Zukunft mit der Entdeckung einer Vielzahl von seltenen neuen Syndromen zu rechnen.
Fanconi-Anämie
Die Fanconi-Anämie ist eine autosomal-rezessiv vererbte Erkrankung mit einer geschätzten Inzidenz von ca. 1:100.000 Einwohner. Als Ursache der Fanconi-Anämie liegen meist Mutationen in Genen vor, die für die Reparatur von DNA-Schäden verantwortlich sind. In jüngeren Jahren zeigt sich die Fanconi-Anämie häufig durch ein Fehlen aller drei Arten von Blutzellen. Klinisch auffällig werden Patienten häufig durch eine Wachstumsstörung (z.B. Kleinwuchs) und Café-au-lait-Flecken (bestimmte Pigmentstörungen) der Haut. Auffälligkeiten an Fingern und Skelett können ebenfalls vorkommen. Diagnostiziert wird die Fanconi-Anämie durch einen so genannten „chromosomal breakage-test“. Im Erwachsenenalter zeigt sich die Fanconi Anämie häufig an allen drei Blutzellarten. Oft zeigen sich bei erwachsenen Patienten keine der typischen körperlichen Symptome. Die korrekte Diagnosestellung der Fanconi-Anämie bei dem Verdacht auf das Vorliegen eines Knochenmarkversagen-Syndroms ist extrem wichtig, da bei diesen Patienten die weiter oben beschriebene immunsuppressive Therapie nicht wirksam ist. Für eine Therapie mit einer Stammzelltransplantation müssen zudem spezielle Fludarabin-haltige (ein bestimmtes Chemotherapeutikum) Behandlungsprotokolle verwendet werden.
Shwachman-Bodian-Diamond-Syndrom
Die Häufigkeit des Shwachman-Bodian-Diamond-Syndrom (SBDS) liegt bei ca. 1:100.000 Einwohnern. Es finden sich auch hier oft verminderte oder fehlende Arten von Blutzellen, sowie ein Kleinwuchs. Dieser entsteht durch eine unzureichende Funktion der Bauchspeicheldrüse. Die Diagnose wird meist im Kindesalter gestellt. Bei Patienten mit schwacher Ausprägung ist damit zu rechnen, dass das Syndrom im Kindes- und Jugendalter unentdeckt bleibt und so bei jungen Patienten mit SBDS eine gewisse Dunkelziffer vorliegt.
Telomeropathien:
Als Telomere werden die Schutzkappen an den Enden der Chromosomen bezeichnet („capping function“). Diese bestehen bei Wirbeltieren aus einer hexamerischen DNA-Komponente mit sich wiederholender Sequenz (TTAGGG). Bei jeder Zellteilung verkürzen sich die Telomere der Tochterzelle bedingt durch das „Endreplikationsproblem“ der DNA-Polymerase, bis schließlich eine kritische Telomerlänge erreicht wird (das sogenannte „Hayflick-limit“) und die Zellen gehen in den Zustand der replikativen Seneszenz über. Die Telomerlänge besitzt dadurch auch die Funktion einer mitotischen Uhr, was Rückschlüsse über die mitotische Vorgeschichte bei verschiedenen Erkrankungen erlaubt.
Gewebe mit einer hohen Zellteilungsrate können dem replikations-abhängigen Verlust der Telomerlänge durch die Aktivierung des Enzyms Telomerase entgegentreten und dadurch länger teilungsfähig bleiben. Diese Aktivierung ist essenziell, da eine Störung zu einer vorzeitigen Verkürzung der Telomere führt. Dies führt schließlich dazu, dass die Gewebsstammzellen zu früh in Seneszenz gehen und das Gewebe vorzeitig altert. Die Telomerlängen werden generell als Marker des biologischen Alters eines Individuums angesehen bzw. die Telomerlänge spiegelt die bisherige replikative Vorgeschichte einer Zelle wider.
Telomeropathien sind seltene Erkrankungen, die dadurch gekennzeichnet sind, dass sich die Telomere auf Grund einer Mutation in den für deren Aufrechterhaltung benötigten Gene vorzeitig verkürzen ("premature aging").
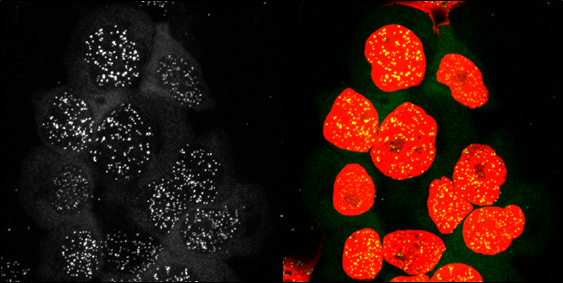
Innerhalb der Gruppe der Telomeropathien gibt es verschiedene Störungen, die vererbt werden können. Beispielsweise kann die Mutation im Enzym Telomerase selbst (hTERC oder hTERT) liegen, aber auch Gene, welche Proteine, die an die Telomerase binden und für die korrekte Funktion notwendig sind, können mutiert sein (DKC1, NHP2, NOP10). Weiter sind Mutationen am Shelterinkomplex (TIN2, TPP1) bekannt oder es kann eine Störung des Transporterproteins der Telomerase (TCAP) vorliegen. Zuletzt existiert noch die Gruppe der Helicasen, welche für die korrekte Synthese der Telomere wichtig sind (RTEL1, CTR1). Das Vererbungsmuster ist meist autosomal dominant, es gibt jedoch auch X-chromosomal vererbte Varianten.
Gemeinsam ist allen Mutationen, dass sie mit einer beschleunigten Telomerverkürzung assoziiert sind. Als Folge kommt es zu einer vorzeitigen Alterung, insbesondere der Hämatopoese, der Leber und Lunge. Aber auch anderer Organe wie die Haut, Schleimhäute und Nägel, die normalerwiese ständig auf nachwachsende und erneuernde Zellen angewiesen sind, weisen Störungen und vorzeitige Alterungserscheinungen auf. Die bisher bekannten und oben erwähnten Gene werden für 50% der Fälle von Dyskeratosis congenita (siehe unten) verantwortlich gemacht. Das gemeinsame diagnostische Kennzeichen aller klinischen Telomeropathieformen sind deutlich verkürzte Telomere gegenüber altersentsprechenden gesunden Kontrollen (< 1-%-Perzentile).
Telomeropathien stellen eine Multi-Systemerkrankung dar und können in drei Krankheitsvarianten eingeteilt werden, von denen die klassische (2.) und die kryptische (3.) Variante im Erwachsenenalter vorkommen können:
- Die schwerverlaufende Variante, auch Revesz-Syndrom oder Hoyeraal–Hreidarsson-Syndrom genannt: Klinisch zeigen die Patienten bereits im frühen Kindesalter ein aplastisches Syndrom mit Knochenmarkversagen und häufig ein nicht voll entwickeltes Kleinhirn sowie Wachstumsstörungen. Diese Varianten gehen mit einer hohen Letalität einher und treten nicht im Erwachsenenalter auf.
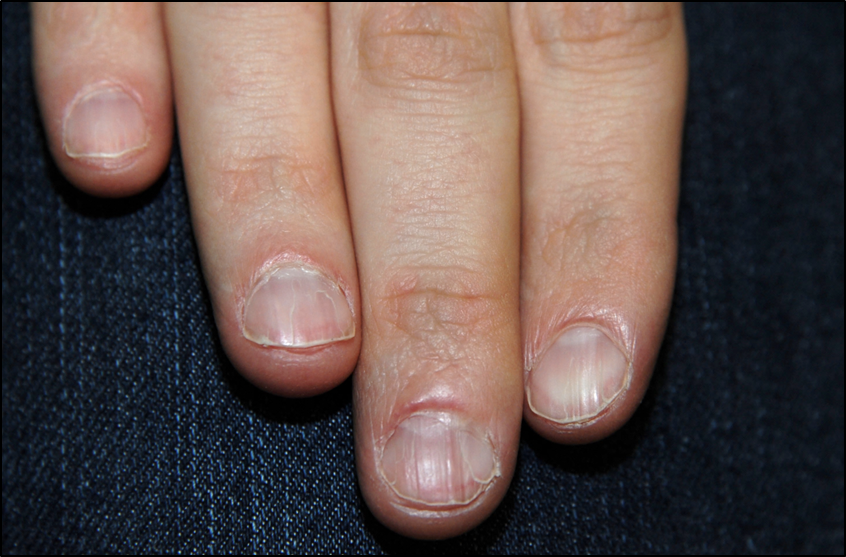
- Die klassische Variante, auch Dyskeratosis congenita (DKC) genannt: klinisch zeigen die Patienten im Jugend- bzw. jungen Erwachsenenalter (bis zum ca. 40. Lebensjahr) ein aplastisches Syndrom mit Knochenmarkversagen (ein sogenanntes hereditäres aplastisches Syndrom) und Hautveränderungen (Nageldystrophie, Leukoplakie und Pigmentstörungen). Ferner sind Lungenfibrose/Emphyseme, Leberzirrhosen oder Enteropathien bekannt.
- Die kryptische Variante: klinisch zeigen die Patienten im späteren Erwachsenenalter nur ein Symptom der DKC, am häufigsten ein alleiniges aplastisches Syndrom mit Knochenmarkversagen, häufig aber auch Lungenerkrankungen wie z.B. Lungenfibrose/Lungenemphysem. Zusätzlich besteht bei Patienten mit Telomeropathie auch ein erhöhtes Risiko für bösartige Erkrankungen z.B. AML/MDS Syndrome, was sich bei diesen Patienten auch als Erstmanifestation zeigen kann.
Diagnosestellung von Telomeropathien:
Aktuell existieren keine Konsensuskritieren zur Diagnosestellung einer Telomeropathie. Die Diagnostik erfolgt unter Berücksichtigung der Telomerlängen, der Klinik, der Familienanamnese und des molekularen Befundes. In Zweifelsfällen können diese Patienten in unserer interdisziplinären Sprechstunde konsiliarisch vorgestellt werden.
Therapeutische Konsequenzen aus der Diagnose einer Telomeropathie:
Sollte bei einem Patienten eine Telomererkrankung oder eine Telomeropathie diagnostiziert werden, so hat dies im Einzelfall weitreichende Konsequenzen. Liegt ein als ideopathische Aplastische Anämie gewertetes „bone marrow failure syndrome“ auf dem Boden einer Telomeropathie vor, so ist bei diesen Patienten aufgrund der Pathophysiologie, der vorzeitigen replikativen Erschöpfung des hämatopoetischen Stammzellpools, nicht mit einem Ansprechen auf eine immunsuppressive Therapie zu rechnen.
Aufgrund des Systemcharakters der Erkrankung muss im Fall einer Organtransplantation (Lunge, Leber oder hämatopoetische Stammzellen) mit verschiedensten zusätzlichen Komplikationen gerechnet werden. Im Falle einer allogenen Stammzelltransplantation ist es äußerst wichtig, die richtige vorbereitende Chemotherapie vor Transplantation auszuwählen, da diese einen Einfluss auf das Gesamtüberleben hat. Wichtig ist hier auch eventuell betroffene Familienspender zu identifizieren und als Spender auszuschließen.
Zusätzlich besteht mittlerweile auch die Möglichkeit einer zielgerichteten Therapie mithilfe von Testosteronderivaten, wie z. B. Danazol, welche zu einer gezielten Erhöhung der Telomeraseaktivität und somit zu einer zumindest partiellen Reversibilität der klinischen Symptomatik mit Verbesserung der Zytopeniesymptomatik führen kann.
Eine rechtzeitige Diagnose ist somit essentiell für eventuelle Therapieentscheidungen und das Management von Nebenwirkungen.
Flow-FISH
Mittels der sogenannten flow-FISH Methode ist ein zügiges Screening auf eine Telomeropathie und ggf. auch der Ausschluss der Erkrankung möglich. Neuere Daten konnten zeigen, dass die große Mehrheit von anderen angeborenen BMFS auch mit einer verkürzten Telomerlänge einhergeht, so dass sich die flow-FISH Technik auch als Screeninginstrument für die angeborenen Nicht-Telomeropathie bedingten Syndrome eignet. Diese Technik ist aktuell der Gold-Standard zum Screening und der Diagnose der Telomeropathien und ist anderen Techniken, wie z.B. der PCR-Technik nachweislich überlegen. Mit dem flow-FISH, welcher in Aachen seit Jahren standardisiert implementiert ist, werden die Telomerlängen in Granulozyten und Lymphozyten bestimmt. Liegen die Telomerlängen im Vergleich zu gesunden Kontrollen unterhalb der sogenannten 1%-Perzentile, liegt mit einer erhöhten Wahrscheinlichkeit auch eine Telomererkrankung vor, da verkürzte Telomere indirekt die Funktionsweise des Telomerasekomplexes bzw. der der altersentsprechenden Aufrechterhaltung der Telomere (sog. „telomere maintenance“) abbilden. Weiter konnte gezeigt werden, dass auch andere angeborene Erkrankungen mit verkürzten Telomeren einhergehen und die Telomeruntersuchung gut geeignet ist, Patienten zu identifizieren bei denen eine erweiterte genetische Untersuchung sinnvoll ist.
NGS „Next Generation Sequencing (NGS)“ und Whole exome Sequencing:
Mithilfe von NGS oder Whole exome Sequencing (WES) werden im Rahmen eines Forschungsvorhabens in Kooperation mit dem Institut für Humangenetik und Genommedizin der Uniklinik RWTH Aachen alle Proben mit Verdacht auf eine angeborene Ursache genetisch untersucht. Diese zusätzliche Untersuchung hilft im jeweiligen Einzelfall die Diagnostik zu komplettieren und die richtige Diagnose zu stellen.
Um die Entwicklung in der Diagnostik, Therapie und Versorgung bei Patienten mit seltenen Erkrankungen weiter zu verbessern, ist die systematische Erfassung in einem krankheitsspezifischen Register unabdingbar. Nur so können auch bei seltenen Erkrankungen repräsentative Aussagen zu Risikofaktoren, möglichen prognostischen Faktoren und vor allem Therapieerfolgen gemacht werden, sowie Nebenwirkungen erfasst und erkannt werden.
Für Patienten mit Telomeropathien (TBD) gab es bis zur Einführung des Aachener Telomeropathie-Registers 2015 beispielsweise keine entsprechenden Register-Daten. Untersuchungen zu Therapieansätzen, Nebenwirkungen und psycho-sozialen Auswirkungen durch die Beschwerden der Erkrankungen, wurden bis dato überhaupt nicht erfasst.
Das Register für Aplastische Anämien und "Bone-Marrow-Failure Syndrome" (AA-BMF-Register) existiert seit 2021 und ist als Weiterentwicklung aus dem 2015 etablierten Aachener Telomeropathie-Register hervorgegangen. Wir bedanken uns bei der Stiftung Lichterzellen für die finanzielle Unterstützung.
In das AA-BMF-Register werden, neben Patienten mit AA und AA/PNH-Overlap Syndromen, auch Patienten mit seltenen angeborenen aplastischen Syndromen eingeschlossen. Dazu zählen beispielsweise die Telomeropathien, aber auch alle anderen Formen von Erkrankungen, die nicht zu dieser Gruppe der Telomeropathien gehören.
Ein Ziel des AA-BMF-Registers ist die Dokumentation klinischer Parameter im Langzeitverlauf. Neben der Telomerlänge und der genetischen Analyse, ist die Analyse des Krankheitsverlaufs essentiell für die Entwicklung neuer prädiktiver und prognostischer Marker. Langfristig ist das Ziel neue Behandlungsstrategien zu entwickeln und die Versorgung der Patienten zu verbessern.
Neben der zentralen Registrierung der Patienten befindet sich am Uniklinikum RWTH Aachen auch die in dieser Form in Europa einzigartige Diagnostikplattform für Telomererkrankungen. Dabei sollen, neben neuesten diagnostischen Methoden, auch neue innovative Therapiestudien den Patienten zur Verfügung gestellt werden.
Wenn Sie Interesse an einer Teilnahme am AA-BMF-Register als Prüfzentrum haben, wenden Sie sich bitte an einen der unter 6. genannten Ansprechpartner.
Es besteht selbstverständlich weiterhin die Möglichkeit der kostenpflichtigen Telomer-Diagnostik über die Firma Repeat Dx.
Prüfzentren des AA-BMF-Registers
Aufgrund der Seltenheit des Krankheitsbildes sollten alle Patienten mit einer aplastischen Anämie oder einem Bone Marrow Failure Syndrom an einem entsprechenden spezialisierten Zentrum vorgestellt werden. Wenn Sie Informationen über die teilnehmenden Prüfzentren in Ihrer Nähe haben möchten (als einweisender Arzt oder als Patient), wenden Sie sich bitte an einen der unter 6. genannten Ansprechpartner.
Seit Jahren gibt es an der Uniklinik RWTH Aachen verschiedene Spezialsprechstunden für Patienten mit aplastischer Anämie und paroxysmaler nächtlicher Hämoglobinurie.
Darüber hinaus ist seit August 2016 die Vorstellung in einer zusätzlichen interdisziplinären Sprechstunde für Patienten mit angeborenen Formen von Knochenmarkversagen-Erkrankungen (Bone Marrow Failure Syndrome, BMFS) möglich.
Ziel dieser Sprechstunde ist es, dem Multisystemaspekt der Erkrankungen, die die Einbeziehung verschiedener ärztlicher Fachbereiche nötig macht, gerecht zu werden. Innerhalb des interdisziplinären Teams werden, abhängig von der Symptomatik, Spezialisten aus den Fachrichtungen Pulmonologie (Med. Klinik I), Hepatologie (Med. Klinik III), Allgemeinchirurgie mit Transplantationserfahrung, Pädiatrie, Humangenetik und Hämato-Onkologie (Med. Klinik IV) hinzugezogen.
Übersicht Ansprechpartner:
Gesamtleitung AA-BMF Schwerpunkt:
Prof. Dr. med. Tim H. Brümmendorf
Telefon: +49 241 80-89806
Fax: +49 241 80-82449
fbeierukaachende
Telomerdiagnostik und Befunde:
Lucia Vankann und Anne Abels
Telefon: +49 241 80-88146
Fax: +49 241 80-82156
lvankannukaachende
aabelsukaachende
telomeropathieukaachende
Sprechstunde für Aplastische Anämien und Aplastische Syndrome (inklusive angeborene Syndrome wie z. B. Telomeropathien):
PD Dr. med. Fabian Beier
Telefon: +49 241 80-89806
Fax: +49 241 80-82156
fbeierukaachende
Sprechstunde für Paroxysmale Nächtliche Hämoglobinurie, AA/PNH Overlap Syndrome und autoimmunhämolytische und unklare Anämieformen
PD Dr. med Jens Panse
Telefon: +49 241 80-89806
Fax: +49 241 80-82156
jpanseukaachende
AA-BMF-Register:
Kim Kricheldorf und Joelle Schifflers
Telefon: +49 241 80-37029/-38664
Fax: +49 241 80-82449
kkricheldorfukaachende
jschifflersukaachende
Wissenschaftliche Arbeitsgruppe „Telomerbiologie und bone marrow failure syndromes“:
PD Dr. med. Fabian Beier
Telefon: +49 241 80-89806
Fax: +49 241 80-82156
fbeierukaachende
Eine Übersicht über die aktiven Studien finden Sie hier.
Eine Übersicht über unsere Forschungsschwerpunkte finden Sie hier.
“Interstitial lung diseases associated with mutations of poly(A)-specific ribonuclease: A multicentre retrospective study.”
Philippot Q, Kannengiesser C, Debray MP, Gauvain C, Ba I, Vieri M, Gondouin A, Naccache JM, Reynaud-Gaubert M, Uzunhan Y, Bondue B, Israël-Biet D, Dieudé P, Fourrage C, Lainey E, Manali E, Papiris S, Wemeau L, Hirschi S, Mal H, Nunes H, Schlemmer F, Blanchard E, Beier F, Cottin V, Crestani B, Borie R; OrphaLung Network.
Respirology. 2022 Jan 3.
“Determinants of survival after lung transplantation in telomerase-related gene mutation carriers: A retrospective cohort.”
Phillips-Houlbracq M, Mal H, Cottin V, Gauvain C, Beier F, Sicre de Fontbrune F, Sidali S, Mornex JF, Hirschi S, Roux A, Weisenburger G, Roussel A, Wémeau-Stervinou L, Le Pavec J, Pison C, Marchand Adam S, Froidure A, Lazor R, Naccache JM, Jouneau S, Nunes H, Reynaud-Gaubert M, Le Borgne A, Boutboul D, Ba I, Boileau C, Crestani B, Kannengiesser C, Borie R; OrphaLung Network.
Am J Transplant. 2021 Dec 1.
“Gain-of-Function Mutations in RPA1 Cause a Syndrome with Short Telomeres and Somatic Genetic Rescue.”
Sharma R, Sahoo SS, Honda M, Granger SL, Goodings C, Sanchez L, Künstner A, Busch H, Beier F, Pruett-Miller SM, Valentine M, Fernandez AG, Chang TC, Géli V, Churikov D, Hirschi S, Pastor VB, Boerries M, Lauten M, Kelaidi C, Wlodarski MW, Cooper MA, Nicholas SK, Rosenfeld JA, Polychronopoulou S, Kannengiesser C, Saintome C, Niemeyer CM, Revy P, Wold MS, Spies M, Erlacher M, Coulon S, Wlodarski MW.
Blood. 2021 Nov 12:blood.2021011980.
Diagnosis and Therapy of aplastic anemia - update 2021.
Panse J.
Dtsch Med Wochenschr. 2021 Apr;146(7):451-454.
“Pegcetacoplan versus Eculizumab in Paroxysmal Nocturnal Hemoglobinuria”
Hillmen P, Szer J, Weitz I, Röth A, Höchsmann B, Panse J, Usuki K, Griffin M, Kiladjian JJ, de Castro C, Nishimori H, Tan L, Hamdani M, Deschatelets P, Francois C, Grossi F, Ajayi T, Risitano A, Peffault de la Tour R.
N Engl J Med. 2021 Mar 18;384(11):1028-1037.
“Treatment of telomeropathies”. (Review)
Vieri M, Brümmendorf TH, Beier F.
Best Pract Res Clin Haematol. 2021 Jun;34(2):101282
“Transient elastography in adult patients with cryptic dyskeratosis congenita reveals subclinical liver fibrosis: a retrospective analysis of the Aachen telomere biology disease registry”
Tometten M, Kirschner M, Isfort S, Berres ML, Brümmendorf TH, Beier F.
Orphanet J Rare Dis. 2021 Sep 26;16(1):395.
“Internet-based patient survey on the consequences of COVID-19 lockdown on treatment and medical follow-up of patients with aplastic anemia or paroxysmal nocturnal hemoglobinuria in Germany.”
Beier F, Kricheldorf K, Burmester P, Göbel U, Isfort S, Panse J, Brümmendorf TH.
Eur J Haematol. 2021 May;106(5):740-742
“Androgen derivatives improve blood counts and elongate telomere length in adult cryptic dyskeratosis congenita.”
Kirschner M, Vieri M, Kricheldorf K, Ferreira MSV, Wlodarski MW, Schwarz M, Balabanov S, Rolles B, Isfort S, Koschmieder S, Höchsmann B, Panse J, Brümmendorf TH, Beier F.
Br J Haematol 2020 Aug 3. doi: 10.1111/bjh.16997.
“PRDM8 reveals aberrant DNA methylation in aging syndromes and is relevant for hematopoietic and neuronal differentiation.”
Cypris O, Eipel M, Franzen J, Rösseler C, Tharmapalan V, Kuo CC, Vieri M, Nikolić M, Kirschner M, Brümmendorf TH, Zenke M, Lampert A, Beier F*, Wagner W*. (*equally contributed)
Clin Epigenetics 2020 Aug 20;12(1):125.
“Comparable Effects of the Androgen Derivatives Danazol, Oxymetholone and Nandrolone on Telomerase Activity in Human Primary Hematopoietic Cells from Patients with Dyskeratosis Congenita.“
Vieri M, Kirschner M, Tometten M, Abels A, Rolles B, Isfort S, Panse J, Brümmendorf TH, Beier F.
Int J Mol Sci. 2020 Sep 29;21(19):E7196.
„Revesz syndrome revisited“
Karremann M, Neumaier-Probst E, Schlichtenbrede F, Beier F, Brümmendorf TH, Cremer FW, Bader P, Dürken M.
Orphanet J Rare Dis. 2020 Oct 23;15(1):299.
“The complement C5 inhibitor crovalimab in paroxysmal nocturnal hemoglobinuria”.
Röth A, Nishimura JI, Nagy Z, Gaàl-Weisinger J, Panse J, Yoon SS, Egyed M, Ichikawa S, Ito Y, Kim JS, Ninomiya H, Schrezenmeier H, Sica S, Usuki K, Sicre de Fontbrune F, Soret J, Sostelly A, Higginson J, Dieckmann A, Gentile B, Anzures-Cabrera J, Shinomiya K, Jordan G, Biedzka-Sarek M, Klughammer B, Jahreis A, Bucher C, Peffault de Latour R.
Blood. 2020 Mar 19;135(12):912-920. doi: 10.1182/blood.2019003399.
“Late-onset and long-lasting autoimmune neutropenia: an analysis from the Italian Neutropenia Registry.”
Fioredda F, Rotulo GA, Farruggia P, Dagliano F, Pillon M, Trizzino A, Notarangelo L, Luti L, Lanza T, Terranova P, Lanciotti M, Ceccherini I, Grossi A, Porretti L, Verzegnassi F, Mastrodicasa E, Barone A, Russo G, Bonanomi S, Boscarol G, Finocchi A, Veltroni M, Ramenghi U, Onofrillo D, Martire B, Ghilardi R, Giordano P, Ladogana S, Marra N, Zanardi S, Beier F, Miano M, Dufour C.
Blood Adv. 2020 Nov 24;4(22):5644-5649.
“Comparison of flow-FISH and MM-qPCR telomere length assessment techniques for the screening of telomeropathies”
Ferreira MSV, Kirschner M, Halfmeyer I, Estrada N, Xicoy B, Isfort S, Vieri M, Zamora L, Abels A, Bouillon AS, Begemann M, Schemionek M, Maurer A, Koschmieder S, Wilop S, Panse J, Brümmendorf TH, Beier F.
Ann N Y Acad Sci. 2019 Oct 24. doi: 10.1111/nyas.14248.
“Design and development of a disease-specific quality of life tool for patients with aplastic anaemia and/or paroxysmal nocturnal haemoglobinuria (QLQ-AA/PNH)-a report on phase III.”
Niedeggen C, Singer S, Groth M, Petermann-Meyer A, Röth A, Schrezenmeier H, Höchsmann B, Brümmendorf TH, Panse J.
Ann Hematol. 2019 Jul;98(7):1547-1559.
“Recurrent somatic mutations are rare in patients with cryptic dyskeratosis congenita”
Kirschner M, Maurer A, Wlodarski M, Ventura Ferreira MS, Bouillon AS, Halfmeyer I, Blau W, Kreuter M, Rosewich M, Corbacioglu S, Beck J, Schwarz M, Bittenbring J, Radsak MP, Wilk CM, Koschmieder S, Begemann M, Kurth I, Schemionek M, Brümmendorf TH, Beier F
Leukemia 2018 Aug;32(8):1762-1767
“DNA methylation in PRDM8 is indicative for dyskeratosis congenita”
Weidner CI, Qiong L, Birkhofer C, Gerstenmaier U, Kaifie A, Kirschner M, Bruns H, Balabanov S, Trummer A, Stockklausner C, Höchsmann B, Schrezenmeier H, Wlodarski M, Panse J, Brümmendorf TH, Beier F*, Wagner W* (*equally contributed)
Oncotarget , accepted 09.02.2016, in press.
Pan-)cytopenia as first manifestation of kryptic telomeropathies in adults
Schmitt K, Beier F, Panse J, Brümmendorf TH.
Dtsch Med Wochenschr . 2016 Oct;141(21):1578-1580. Review
“Early-onset Evans syndrome, immunodeficiency, and premature immunosenescence associated with tripeptidyl-peptidase II deficiency”
Stepensky P, Rensing-Ehl A, Gather R, Revel-Vilk S, Fischer U, Nabhani S, Beier F, Brümmendorf TH, Fuchs S, Zenke S, Firat E, Pessach VM, Borkhardt A, Rakhmanov M, Keller B, Warnatz K, Eibel H, Niedermann G, Elpeleg O, Ehl S.
Blood, 2015 Jan 29;125(5):753-61
“Telomere shortening in enterocytes of patients with uncontrolled acute intestinal graft-versus-host disease”
Hummel S, Ventura Ferreira MS, Heudobler D, Huber E, Fahrenkamp D, Gremse F, Schmid K, Müller-Newen G, Ziegler P, Jost E, Blasco MA, Brümmendorf TH, Holler E, Beier F.
Blood, 2015 Nov 26;126(22):2518-21
“A novel autosomal recessive TERT T1129P mutation in a dyskeratosis congenita family leads to cellular senescence and loss of CD34+ hematopoietic stem cells not reversible by mTOR-inhibition”
Stockklausner C, Raffel S, Klermund J, Bandapalli OR, Beier F, Brümmendorf TH, Bürger F, Sauer SW, Hoffmann GF, Lorenz H, Tagliaferri L, Nowak D, Hofmann WK, Buergermeister R, Kerber C, Rausch T, Korbel JO, Luke B, Trumpp A, Kulozik AE.
Aging (Albany NY), 2015 Nov;7(11):911-27
“Rps14 haploinsufficiency causes a block in erythroid differentiation mediated by S100A8/S100A9”
Schneider RK, Schenone M, Ventura Ferreira M, Kraman R, Joyce CE, Hartigan C, Beier F, Brümmendorf TH, Germing U, Platzbecker U, Büsche G, Knüchel R, Chen MC, Waters CS, Chen E, Chu LP, Novina CD, Lindsley RC, Carr SA, Ebert BL.
Nature Medicine, accepted 19.12.2015, in press.
“Chronic replicative stress induced by CCl4 in TRF1 knockout mice recapitulates the origin of large liver cell changes”
Beier F, Martinez P, Blasco MA.
J Hepatol . 2015 Aug;63(2):446-55
“Therapeutic effect of androgen therapy in a mouse model of aplastic anemia produced by short telomeres”
Bär C, Huber N, Beier F, Blasco MA.
Haematologica . 2015 Oct;100(10):1267-74
“Reconstructing the in vivo dynamics of hematopoietic stem cells from telomere length distributions”
Werner B*, Beier F*(*equally contributed), Hummel S, Balabanov S, Lassay L, Orlikowsky T, Dingli D, Brümmendorf TH, Traulsen A.
Elife, 2015 Oct 15;4.
“Genetic characterization of acquired aplastic anemia by targeted sequencing”
Heuser M, Schlarmann C, Dobbernack V, Panagiota V, Wiehlmann L, Walter C, Beier F, Ziegler P, Yun H, Kade S, Kirchner A, Huang L, Koenecke C, Eder M, Brümmendorf TH, Dugas M, Ganser A, Thol F.
Haematologica 2014 Sep;99(9):e165-7.
“Telomere elongation and clinical response to androgen treatment in a patient with aplastic anemia and a heterozygous hTERT gene mutation.”
Ziegler P, Schrezenmeier H, Akkad J, Brassat U, Vankann L, Panse J, Wilop S, Balabanov S, Schwarz K, Martens UM, Brümmendorf TH.
Ann Hematol. 2012 Jul;91(7):1115-20

